以下是一些常用的危险品标志,装运酒精的包装箱应贴的图标是
下列有关胶体的叙述中不正确的是
| A.淀粉溶胶中胶体微粒直径大小在1~100nm |
| B.用一束光照射氢氧化铁胶体,可以观察到一条光亮的通路 |
| C.向烧杯中沸腾的蒸馏水里加几滴FeCl3饱和溶液,继续煮沸至液体呈红褐色,停止加热可得氢氧化铁胶体 |
| D.可以利用过滤操作来分离胶体粒子和溶液 |
将碘水中的碘萃取出来的实验中,下列说法错误的是
| A.分液漏斗使用前要检查它是否漏水 |
| B.要求萃取剂既不溶于水,且比水更容易使碘溶解 |
| C.分液漏斗注入碘水和萃取剂,反复倒转并用力振荡后,不必静置,应立即分液 |
| D.分液时,下层液体应从下口放出,上层液体应从上口倒出 |
下列能导电的物质是
| A.固态NaOH | B.酒精 | C.液态氯化氢 | D.NaCl溶液 |
能区别硝酸银、盐酸、氢氧化钾三种溶液的一种试剂是
| A.MgCl2溶液 | B.FeCl3溶液 | C.NaNO3溶液 | D.K2SO4溶液 |
下列基本实验操作中,正确的是
下列括号中的分离方法运用得当的是
| A.植物油和水(蒸馏) | B.水溶液中的食盐和碘(分液) |
| C.CaCO3和CaCl2(溶解、过滤、蒸发) | D.自来水中的杂质(萃取) |
下列物质中,摩尔质量最大的是
| A.H2O | B.H2SO4 | C.Al | D.CaCO3 |
下列说法正确的是
| A.等体积的O2和N2中的分子数相等 |
| B.等温等压的NO和CH4中的分子数相等 |
| C.20℃等压等体积的O2和O3中的分子数相等 |
| D.等压的N2和CO2中的分子数 |
下列溶液中的c(Cl-)与50 mL 1 mol/L FeCl3溶液中的c(Cl-)相等的是
| A.1 mol/L NaCl溶液 | B.2 mol/L NH4Cl溶液 |
| C.1.5 mol/L MgCl2溶液 | D.2 mol/L AlCl3溶液 |
下列过程中涉及化学变化的是
| A.蒸馏法将海水淡化为饮用水 |
| B.三氯化铁溶液滴入沸水中制胶体 |
| C.渗析法除去淀粉溶胶中的NaCl |
| D.向Fe(OH)3胶体中加入MgSO4溶液产生沉淀 |
下列对应化学反应的离子方程式书写正确的是
| A.氢氧化铁与盐酸反应:H++OH-===H2O |
| B.Ca(HCO3)2溶于稀盐酸中:CO32-+2H+===CO2↑+H2O |
| C.铁与H2SO4反应:Fe+2H+===Fe3++H2↑ |
| D.澄清的石灰水与醋酸反应:OH-+CH3COOH=CH3COO-+H2O |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.强酸性溶液中:Mg2+、K+、SO42-、NO3- |
| B.强碱性溶液中:Na+、Cu2+、HCO3-、NO3- |
| C.AgNO3溶液中:H+、K+、SO42-、Cl- |
| D.Ba(NO3)2溶液中:Mg2+、K+、SO42-、Cl- |
下列电离方程式中,正确的是
| A.Na2SO4 = 2Na+ + SO4-2 | B.H2CO3 = 2H++ CO32- |
| C.Al2(SO4) 3 = 2Al3++ 3SO42- | D.Ca(NO3)2= Ca2+ + 2(NO3) 2- |
下列反应不能用离子方程式CO32-+2H+=CO2↑+H2O表示的是
| A.Na2CO3+2HCl=2NaCl+CO2↑+H2O | B.BaCO3+2HCl=BaCl2+H2O+CO2↑ |
| C.K2CO3+H2SO4=K2SO4+CO2↑+H2O | D.K2CO3+2HNO3=2KNO3+CO2↑+H2O |
下列溶液中溶质的物质的量浓度为l mol/L的是
| A.将40 g NaOH固体溶解于1 L水中 |
| B.将22.4 L氯化氢气体溶于水配成l L溶液 |
| C.将l L 10 mol/L的浓盐酸与9 L水混合 |
| D.20 g NaOH固体溶解在水中配成500 mL溶液 |
过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4等杂质,通过如下几个实验步骤,可制得食盐水:①加入稍过量的Na2CO3溶液;②加入稍过量的NaOH溶液;③加入稍过量的BaCl2 溶液;④滴入稀盐酸至无气泡产生;⑤过滤
正确的操作顺序是
| A.③②①⑤④ | B.①②③⑤④ | C.②③①④⑤ | D.③⑤②①④ |
下列物质的分类正确的是
| |
单质 |
酸性氧化物 |
碱性氧化物 |
酸 |
碱 |
盐 |
| A |
H2 |
干冰 |
CuO |
H2SO4 |
纯碱 |
小苏打 |
| B |
碘酒 |
CO |
Na2O |
HCl |
NH3·H2O |
NaCl |
| C |
液氮 |
SO2 |
Mn2O7 |
醋酸 |
乙醇 |
胆矾 |
| D |
金刚石 |
P2O5 |
生石灰 |
HNO3 |
KOH |
CaCO3 |
NA表示阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,1mol Cl2和HCl的混合气体所含分子总数为2NA |
| B.101kPa 、0℃时,22.4 LH2中氢原子数为NA个 |
| C.标准状况下,2.24 L CCl4含有的碳原子数目为0.1NA |
| D.常温常压下3.2 g O2中含有的氧原子数目为0.2 NA |
如果a g某气体中含有的分子数为b,则c g该气体在标准状况下的体积是(式中NA为阿伏加德罗常数)
A. |
B. |
C. |
D. |
I.用下列仪器的编号回答问题:
①容量瓶 ②蒸馏烧瓶 ③量筒 ④烧杯 ⑤托盘天平 ⑥分液漏斗
(1)可加热的仪器且加热时必须垫石棉网的有 ;
(2)使用前必须检查是否漏水的有 ;
(3)仪器上标有零刻度的有 。
II.草木灰中富含钾盐,主要成分是碳酸钾,还含有少量氯化钾和硫酸盐。现从草木灰中提取钾盐,并用实验检验其中的 CO32-、 SO42-、 和 Cl-。
(1)从草木灰中提取钾盐的实验操作顺序如下:①称取样品;②溶解沉降;③ ;④ ;⑤冷却结晶。
(2)在进行上述②、③、④ 操作时,都要用到玻璃棒,其作用分别是:
② ;③ ;④ 。
(3)将制得的少量晶体放入试管,加入蒸馏水溶解并把溶液分成二份,分装在2支试管里。①在第一支试管里加入稀盐酸,可观察有 生成,证明溶液中有 离子。②在第二支试管里加入足量稀硝酸后,再加入足量Ba(NO3)2溶液,可观察到有 生成,证明溶液中有 离子。③将第二支试管反应后的溶液过滤,在滤液里加入AgNO3溶液,可观察到有 生成,证明溶液中有 离子。
(4)用托盘天平称量样品时,若指针偏向右边,则表示 (填选项的标号)。
| A.左盘重,样品轻 | B.左盘轻,砝码重 |
| C.右盘重,砝码轻 | D.右盘轻,样品重 |
按要求写方程式。
(1)碳酸钙和盐酸(写出离子方程式)
(2)氢氧化钡溶液和稀硫酸(写出离子方程式)
(3)Fe2(SO4)3(写出电离方程式)
(4)H+ + OH- = H2O(写出对应的化学方程式)
(5)将下列离子Na+、K+、Cu2+、H+、NO3-、Cl-、CO32-、OH-按可能大量共存于同一溶液的情况,把他们分成A、B两组,而且每组中均含两种阳离子和两种阴离子。
A组:Cu2+和
B组:
实验室需要用NaOH固体配制0.1mol/LNaOH溶液450mL和用浓硫酸配制0.5mol/L的硫酸溶液500mL。根据这两种溶液的配制情况回答下列问题。
(1)在下图所示仪器中,配制上述溶液肯定不需要的是_________(填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是 。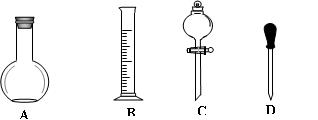
(2)在容量瓶的使用方法中,下列操作不正确的是____________
| A.容量瓶洗涤后残留少量水不影响使用 |
| B.容量瓶用水洗净后,再用待配溶液洗涤 |
| C.配制NaOH溶液时,如果试样是固体,把称好的固体用纸条小心倒入容量瓶中,缓慢加水至接近刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线。 |
| D.配制硫酸溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加水至刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线。 |
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次摇匀。
(3)用托盘天平称取NaOH的质量为 g。在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度 0.1mol/L(填“大于”“小于”或“等于”)。
(4)根据计算得知,需用量筒量取质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为 mL(保留到小数点后1位。),若实验室有15mL、20mL、50mL量筒,应选用 mL量筒最好。
某溶液中含有Ba2+,Cu2+,Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离。其中沉淀1和沉淀3为白色,沉淀2为蓝色。流程如右图: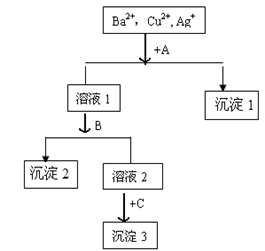
(1)沉淀的化学式:沉淀1 ,沉淀2 ,沉淀3 ;
(2)写出混合液+A反应的离子方程式 ;
溶液+B反应的离子方程式 ;
I.在标准状况下,由CO和CO2组成的混合气体4.48L,质量是8g。此混合物中CO和CO2的物质的量比是 ① ,CO的体积分数是 ② ,CO的质量分数是 ③ ,混合气体中C和O的原子个数比是 ④ ,混合气体的平均摩尔质量是 ⑤ 。
II.现有mg某气体,它由双原子分子构成,它的摩尔质量为M g/mol。若阿伏加德罗常数用NA表示,则:
(1)该气体所含原子总数为________个。
(2)该气体若溶于1L水中(不考虑反应),设溶液的密度为ρg/cm3,则该溶液的物质的量浓度为__________mol·L-1。