以节能减排为基础的低碳经济是保持社会可持续发展的战略举措。下列做法违背发展低碳经济的是
| A. | 发展氢能和太阳能 |
| B. | 限制塑料制品的使用 |
| C. | 提高原子利用率,发展绿色化学 |
| D. | 尽量用纯液态有机物代替水作溶剂 |
化学已渗透到人类生活的各个方面。下列说法不正确的是
| A. | 阿司匹林具有解热镇痛作用 |
| B. | 可以用 、 制作高温结构陶瓷制品 |
| C. |
在入海口的钢铁闸
 门上装一定数量的铜块可防止闸门被腐蚀 门上装一定数量的铜块可防止闸门被腐蚀
|
| D. |
禁止使用四乙基铅作汽油抗爆震剂,可减少
 汽车尾气污染 汽车尾气污染
|
化学与能源开发、环境保护、资源利用等密切相关。下列说法正确的是
| A. | 为提高农作物的产量和质量,应大量使用化肥和农药 |
| B. | 绿色化学的核心是应用化学原理对环境污染进行治理 |
| C. | 实现化石燃料清洁利用,就无需开发新能源 |
| D. | 垃圾是放错地方的资源,应分类回收利用 |
下列有关物质的性质或应用的说法不正确的是
| A. | 二氧化硅是生产光纤制品的基本原料 |
| B. | 水玻璃可用于生产黏合剂和防火剂 |
| C. |
盐析可提
 纯蛋白质并保持其生理活性 纯蛋白质并保持其生理活性
|
| D. | 石油分馏可获得乙烯、丙烯和丁二烯 |
钡盐行业生产中排出大量的钡泥[主要含有、、、 等]。某主要生产、、的化工厂利用钡泥制取,其部分工艺流程如下:

(1)酸溶后溶液的 =1,与的反应化学方程式为。
(2)酸溶时通常控制反应温度不超过70℃,且不使用浓硝酸,原因是。
(3)该厂结合本厂实际,选用的为(填化学式);中和使溶液中(填离子符号)的浓度减少(中和引起的溶液体积变化可忽略)。
(4)上述流程中洗涤的目的是。
下表列出了3种燃煤烟气脱硫方法的原理。

(1)方法Ⅰ中氨水吸收燃煤烟气中的化学反应为:


能提高燃煤烟气中去除率的措施有(填字母)。
A.增大氨水浓度 B.升高反应温度
C.使燃煤烟气与氨水充分接触 D . 通入空气使转化为
. 通入空气使转化为
采用方法Ⅰ脱硫,并不需要预先除去燃煤烟气中大量的,原因是(用离子方程式表示)。
(2)方法Ⅱ重要发生了下列反应:




与反应生成的热化学方程式为。
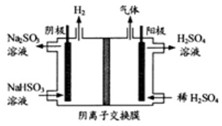
(3)方法Ⅲ中用惰性电极电解溶液的装置如上图所示。阳极区放出气体的成分为。(填化学式)
下列做法不能体现低碳生活的是
| A. | 减少食物加工过程 | B. | 注意节约用电 |
| C. | 尽量购买本地的、当季的食物 | D. | 大量使用薪柴为燃料 |
下列有关物质性质的描述不符合事实的是
| A. | 有机物不导电 | B. | 金刚石是自然界最硬的物质 |
| C. | 可用作食品防腐剂 | D. | 可用于某些疾病的治疗 |
硫酸锌可作为食品锌强化剂的原料。工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是,并含少量的、 、等,生产工艺流程示意如下:

(1)将菱锌矿研磨成粉的目的是。
(2完成"氧化除铁"步骤中反应的离子方程式:
++= +
(3)针铁矿()是以德国诗人歌德()名字命名的,组成元素是、和,化学式量为89,化学式是。
(4)根据下表数据,调节"滤液2"的时,理论上可选用的最大区间为。
| 开始沉淀的 | 10.4 |
6.4 |
- |
- |
| 沉淀完全的 | 12.4 |
8.0 |
- |
- |
| 开始溶解的 | - |
10.5 |
- |
- |
| 5.6×10-12 |
- |
6.8×10-5 |
2.8×10-9 |
(5)工业上从"滤液3"制取过程中,合适的反应物是(选填序号)。
a.大理石粉 b.石灰乳 c.纯碱溶液 d.烧碱溶液
(6)"滤液4"之后的操作依次为、、过滤,洗涤,干燥。
(7)分析图中数据,菱锌矿粉中的质量分数不低于。
玻璃钢可由酚醛树脂和玻璃纤维制成。
(1)酚醛树脂由酚醛和甲醛缩聚而成,反应有大量热放出,为防止温度过高,应向有苯酚的反应釜加入甲醛,且反应釜应装有装置。
(2)玻璃纤维由玻璃拉丝得到。普通玻璃由石英砂、和石灰石(或长石)高温熔融而成,主要反应的化学方程式为。
(3)玻璃钢中玻璃纤维的作用是。玻璃钢具有等优异性能(写出两点即可)
(4)下列处理废旧热固性酚醛塑料的做法合理的是
a.深埋
b.粉碎后用作树脂填料
c.用作燃料
d.用有机溶剂将其溶解,回收树脂
下列物质中,可形成酸雨的是
| A. | 二氧化硫 | B. | 氟氯代烃 | C. | 二氧化碳 | D. | 甲烷 |
Ⅰ固硫剂是把煤燃烧时生成的二氧化硫以盐的形式固定在炉渣中的物质,可减少二氧化硫对大气的污染。下列物质中可用做固硫剂的有
| A. | B. | C. | D. |
Ⅱ以黄铁矿为原料,采用接触法生产硫酸的流程可简示如下:

请回答下列问题:
(1)在炉气制造中,生成的化学方程式为;
(2)炉气精制的作用是将含的炉气、及干燥,如果炉气不经过精制,对催化氧化的影响是 :

(3)精制炉气(含体积分数为7%、为ll%、为82%)中平衡转化率与温度及压强关系如下图所示。在实际生产中,催化氧化反应的条件选择常压、450℃;左右(对应图中点),而没有选择转化率更高的或点对应的反应条件,其原因分别是、;
(4)在催化氧化设备中设置热交换器的目的是、,从而充分利用能源。
节能减排对发展经济、保护环境有重要意义。下列措施不能减少二氧化碳排放的是()
| A. | 利用太阳能制氢 | B. | 关停小火电企业 |
| C. |
举行"地球一小时"熄灯活动

|
D. | 推广使用煤液化技术 |
四川攀枝花蕴藏丰富的钒、钛、铁资源。用钛铁矿渣(主要成分为、、,的最高化合价为+4)作原料,生产白色颜料二氧化钛的 主要步骤如下:
主要步骤如下:

请回答下列问题:
(1)硫酸与二氧化钛反应的化学方程式是。
(2)向滤液I中加入铁粉,发生反应的离子方程式为:、。
(3)在实际生产过程中,向沸水中加入滤液Ⅲ,使混合液达0.5,钛盐开始水解。水解过程中不断通入高温水蒸气,维持溶液沸腾一段时间,钛盐充分水解析出水合二氧化钛沉淀。请用所学化学平衡原理分析通入高温水蒸气的作用:。
过滤分离出水合二氧化钛沉淀后,将滤液返回的主要目的是充分利用滤液中的钛盐、、、(填化学式),减少废物排放。
(4)可用于生产红色颜料(),其方法是:将556(摩尔质量为278 )溶于水中,加入适量氢氧化钠溶液恰好完全反应,鼓入足量空气搅拌,产生红褐色胶体;再向红褐 色胶体中加入3336和112铁粉,鼓入足量空气搅拌,反应完成后,有大量附着在胶体粒子上以沉淀形式析出;过滤后,沉淀经高温灼烧得红色颜料。若所得滤液中溶质只有硫酸钠和硫酸铁,则理论上可生产红色颜料。
色胶体中加入3336和112铁粉,鼓入足量空气搅拌,反应完成后,有大量附着在胶体粒子上以沉淀形式析出;过滤后,沉淀经高温灼烧得红色颜料。若所得滤液中溶质只有硫酸钠和硫酸铁,则理论上可生产红色颜料。
减缓温室气体排放是2009年哥本哈根气候变化会议的议题。下列反应不产生温室气体的是
| A. | 用纯碱制玻璃 | B. | 用煤炭作燃料 |
| C. | 用铁矿石炼铁 | D. | 用氨制碳酸铵 |
水是一种重要的自然资源,是人类赖以生存不可缺少的物质。水质优劣直接影响人体健康。请回答下列问题:
(1)天然水中溶解的气体主要有 、。
(2)天然水在净化处理过程中加入的混凝剂可以是其纯净水作用的原理是
(3)水的纯净和软化的区别是
(4)硬度为的水是指每升水含10或与之相当的物质(如7.1)。若某天然水中,,则此水的硬度为;
(5)若(4)中的天然水还含有,现要软化10这种天然水,则需先加入,后加入。