胶体区别于其它分散系最本质的特征是
| A.外观澄清、透明 | B.胶体粒子直径在1~100nm之间 |
| C.能产生丁达尔现象 | D.外观澄清、不透明 |
当身处贴有下列标志的环境时,行为不正确的是
下列反应不属于氧化还原反应的是
| A.铝片与稀盐酸的反应 | B.Ca(OH)2与NH4Cl的反应 |
| C.灼热的炭与CO2的反应 | D.甲烷在氧气中的燃烧反应 |
下列互为同位素的是
| A.H2O和D2O | B.14N和14C | C.16O和18O | D.金刚石和石墨 |
下列变化属于化学变化的是
| A.碘的升华 | B.碘化银用于人工降雨 |
| C.液溴的挥发 | D.从海水中提取溴 |
下列物质属于电解质的是
| A.CO2 | B.Al | C.Na2SO3 | D.蔗糖 |
氯、溴、碘三种卤素单质的化学性质相似。其原因是
| A.颜色相似 | B.都是双原子分子 |
| C.最外层电子数相同,都是7 | D.自然界中都以化合态存在 |
下列电离方程式错误的是
| A.CaCl2=Ca2+ + 2Cl— | B.H2SO4= 2H+ + SO42— |
| C.NaHCO3= Na++ HCO3— | D.KOH = K+ + O2—+H+ |
下列物质所属类别不正确的是
| A.纯碱——碱 | B.氯化铝——盐 |
| C.金属钠——还原剂 | D.二氧化硅——酸性氧化物 |
下列化学用语正确的是
| A.次氯酸的化学式:HClO2 |
B.硫离子的结构示意图: |
| C.质量数为127的钡原子:127 Ba |
| D.氨气(NH3)中氮元素的化合价:+3 |
实验室中配制250mL 0.10mo1·L-1NaOH溶液时,必须使用到的玻璃仪器是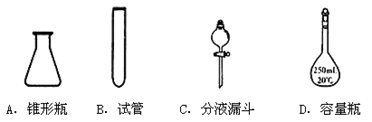
可用分液漏斗分离的一组混合物是
| A.苯和酒精 | B.四氯化碳和溴 | C.苯和水 | D.醋酸和水 |
下列气体有颜色且具有刺激性气味的是
| A.O2 | B.Cl2 | C.NH3 | D.N2 |
下列实验方法或操作正确的是
| A.转移溶液 | B.制蒸馏水 | C.分离水和酒精 | D.稀释浓硫酸 |
下列化合物中,属于碱性氧化物的是
| A.CaO | B.NaOH | C.CO2 | D.Fe3O4 |
下列关于氯气的叙述中不正确的是
| A.可用向上排空气法收集少量的氯气 |
| B.与水反应生成的次氯酸是一种弱酸 |
| C.与石灰乳反应时,Cl2既被还原,同时又被氧化 |
| D.常温下干燥的Cl2能用钢瓶贮运,所以Cl2与铁不能发生化学反应 |
下列元素中,最高正化合价数值最大的是
| A.Cl | B.F | C.S | D.C |
下列实验操作正确的是
| A.用酒精萃取碘水中的碘 |
| B.蒸馏时,应使温度计水银球伸入蒸馏烧瓶内液面下 |
| C.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D.用洁净的铂丝蘸取少量溶液在酒精灯火焰上灼烧,火焰呈黄色,则溶液中一定不含有K+ |
下列实验方法及判断不正确的是
| A.用NaOH溶液来鉴别NH4Cl和KCl |
| B.用硝酸酸化的AgNO3溶液来鉴别NH4Cl和NH4NO3 |
| C.某溶液中滴加BaCl2溶液后产生白色沉淀,则该溶液中一定含有SO42-离子 |
| D.用焰色反应鉴别NaCl和KNO3 |
我国古代就有湿法炼铜的记载“曾青得铁则化为铜”,相关反应的化学方程式为:Fe+CuSO4=Cu+FeSO4。下列有关该反应的说法中正确的是
| A.Fe被氧化 | B.CuSO4是还原剂 |
| C.Fe是氧化剂 | D.CuSO4发生氧化反应 |
某元素二价阴离子的核外有18个电子,质量数为34,该元素的原子核中的中子数为
| A.16 | B.18 | C.20 | D.22 |
下列溶液中NO3-的物质的量浓度最大的是
| A.500 mL 1 mol/L的HNO3溶液 |
| B.1 L 0.5 mol/L的Fe(NO3)3溶液 |
| C.100 mL 0.5 mol/L的Mg(NO3)2溶液 |
| D.300 mL 1 mol/L的Mg(NO3)2溶液 |
用NA表示阿伏加德罗常数的数值,下列说法正确的是
| A.1 mol Cl2与足量的铁反应转移的电子数是2 NA |
| B.常温常压下22.4 L HCl气体含有的分子数是NA |
| C.0.1 mol/L CuCl2溶液中Cl-数目是0.2 NA |
| D.32 g O2中含有的原子数是 NA |
下列说法中不正确的是
| A.在标准状况下,氯气的密度约为3.17g/L |
| B.密闭容器中的氯水放置数天后,PH变小且几乎失去漂白性 |
| C.液氯具有漂白性,干燥的氯气和液氯均能使干燥的有色布条褪色 |
| D.在通常情况下,氯气可以和某些金属直接化合 |
取软锰矿石(主要成分为MnO2)116g 跟足量浓盐酸发生如下反应(杂质不参与反应)MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O,制得22.4L Cl2(标准状况)。下列有关说法中不正确的是
MnCl2+Cl2↑+2H2O,制得22.4L Cl2(标准状况)。下列有关说法中不正确的是
| A.这种软锰矿石中MnO2的质量分数为75% |
| B.被氧化的HCl的物质的量为4mol |
| C.参加反应的HCl的质量为146g |
| D.被还原的MnO2的物质的量为1mol |
(1)化学与人类生产、生活密切相关。请按要求回答下列问题:
①下列我国古代的技术应用中,其工作原理不涉及化学反应的是 (填字母)
| A.火药使用 |
B.粮食酿酒 |
C.转轮排字 |
D.铁的冶炼 |
 |
 |
 |
 |
②下列用品的有效成分及用途对应错误的是 (填字母)
| |
A |
B |
C |
D |
| 用品 |
 |
 |
 |
 |
| 有效成分 |
NaCl |
NaOH |
NaHCO3 |
Ca(ClO)2 |
| 用途 |
做调味品 |
做治疗胃病的抗酸药 |
做发酵粉 |
做消毒剂 |
③工业上常用氯气和石灰乳反应生产漂白粉,其原理是_________________(用化学方程式表示)。
④在生产中,人们曾用浓氨水来检验氯气管道是否漏气。如果氯气管道某处漏气,用浓氨水检查时就会产生白烟的现象,又知此时发生的是有氮气生成的置换反应,则此时发生反应的化学方程式为____________。
(2)科学家在研究化学物质时,常常对物质进行分类,以便对同类物质的组成和性能进行深入的研究。物质分类及转化思想贯穿整个化学科学习的始终。
①有下列十种物质:
A.空气 B.O2 C.NaHSO4 D.氨水 E.CuSO4·5H2O F.NaOH
G.CO2 H.Fe2O3 I.金刚石 J.H2SO4
其中属于混合物的有 ;属于单质的有 ;属于盐的有 。(填字母)
②有下列六个反应:
A.Cl2+H2O = HCl+HClO
B.Zn + H2SO4 = ZnSO4 + H2↑
C.2Cu2O + Cu2S  6Cu+SO2↑
6Cu+SO2↑
D.Cl2+2KI = 2KCl+I2
E.H2 + Cl2 2HCl
2HCl
F.2KClO3 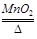 2KCl+3O2↑
2KCl+3O2↑
其中属于置换反应的是 ,既属于分解反应又属于氧化还原反应的是 (填字母)。
③K2FeO4是一种重要的净水剂,可用下列方法制得:
2Fe(OH)3+3Cl2+10KOH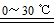 2K2FeO4+6KCl+8H2O
2K2FeO4+6KCl+8H2O
在该反应中,还原剂是 ,当反应中有1mol K2FeO4生成时,转移电子的数目为 。
(3)物质的量是化学计算的核心。请按要求完成下列填空:
①已知3.01×1023个X气体分子的质量为8g,则X气体的摩尔质量是 。
②含0.4 mol Al3+的Al2O3的质量是 。
③某块光卤石(KCl·MgCl2·6H2O)中含5.3250 g Cl—,则该光卤石的物质的量为 。
④标准状况下,224mL的氨气中含有的氢原子数为 。
已知物质A~I之间的转化关系符合下图所示。其中A、C、F、G、I为常见固体且焰色反应均为黄色;A为海水中主要溶质,B为常温下常见液体;E为黄绿色气体,H是无色无味且能使澄清石灰水变浑浊的气体。

试回答下列问题:
(1)写出下列物质的化学式:D H
(2)反应①的化学方程式为: 。
(3)反应②的化学方程式为: 。
结合氯气的相关知识解决下列问题。
(1)在实验室中制取Cl2,下列收集Cl2的装置中正确的是 (填字母)。

(2)漂白粉能与盐酸发生反应,但盐酸浓度不同时,漂白粉与盐酸混合发生反应的类型不同。
漂白粉与稀盐酸发生复分解反应,化学方程式为 。
漂白粉与浓盐酸发生氧化还原反应,化学方程式为 。
(3)实验室可以用MnO2和浓盐酸在加热条件下制备Cl2,还可以用KMnO4与浓盐酸在常温下制备Cl2。高锰酸钾溶液常用于物质的定性检验与定量分析。某化学兴趣小组在实验室里欲用KMnO4固体来配制250.00 mL 0.1000 mol/L的KMnO4溶液。
①需用的仪器有天平、药匙、烧杯、玻璃棒、量筒、胶头滴管、 。
②下列操作会导致实验结果偏小的是 (填字母)。
a.加水定容时俯视刻度线
b.容量瓶内壁附有水珠而未干燥处理
c.颠倒摇匀后发现凹液面低于刻度线又加水补上
(4)氯水中含有多种成分,因而具有很多性质,根据氯水分别与如图四种物质发生的反应填空(a、b、c、d重合部分代表物质间反应,且氯水足量)。

①能证明氯水具有漂白性的是__________(填“a”、“b”、“c”或“d”)。
②c过程中的现象是___________________。