生活中的一些问题常涉及到化学知识,下列叙述正确的是
| A.明矾是常用的水处理剂,可以淡化海水 |
| B.“加碘食盐”、“含氟牙膏”、“富硒营养品”中的碘、氟、硒均以分子形式存在 |
| C.黑火药有硫磺、硝石、木炭三种物质按一定的比例混合而成 |
| D.在食品袋中放入盛有CaCl2 .6H2O和铁粉的透气小袋,可防止食物受潮、氧化变质 |
下列与化学概念有关的说法正确的是
| A.SiO2、P2O5、NO均为酸性氧化物 |
| B.NaH 、NaBH4、NaClO均为离子化合物 |
| C.NH3.H2O是弱碱,所以NH4NO3为弱电解质 |
| D.磁性氧化铁、水玻璃、液氨均为混合物 |
下列物质的使用不涉及化学变化的是
| A.铝热剂焊接钢轨 | B.黏土烧结制陶瓷 |
| C.氢氟酸刻蚀玻璃 | D.甘油作护肤保湿剂 |
下列有关金属及其化合物的说法正确的是
| A.除去MgCl2溶液中少量的FeCl3,可选用MgO |
| B.Na久置与空气中最终生成NaHCO3 |
| C.铝、铁、铜在空气中长时间放置,表面均只生成氧化物 |
| D.向NaOH溶液中逐滴加入少量饱和FeCl3溶液,可制得Fe(OH)3胶体 |
下列与实验相关的叙述,正确的是
| A.浓硝酸存放在带橡胶塞的棕色玻璃瓶中 |
| B.四氯化碳萃取溴水中的溴时,水从分液漏斗下口流出 |
| C.向饱和的NaCl溶液中通入足量的NH3后,再通入CO2,有晶体析出 |
| D.某溶液中滴加BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液中一定含有Ag+ |
设NA为阿伏伽德罗常数的值,下列叙述正确的是
| A.20gH218O和20gD2O中含有的中子数均为10NA |
| B.标准状况下,11.2LO2参加反应转移的电子数一定是2NA |
| C.1L的生理盐水(0.9%NaCl溶液)中含有Na+数为9NA |
| D.标准状况下,分子数为NA的NO2、N2O4混合气体体积约为22.4L,质量为46g |
下列反应对应的离子方程式正确的是
| A.等体积、等浓度的Ca(HCO3)2溶液和NaOH溶液混合: HCO3- + Ca2++OH-=CaCO3↓+H2O |
| B.过氧化钠溶于水:2022-+2H2O=4OH-+O2↑ |
| C.用MnO2从酸化的海带灰中浸取液中提取碘:MnO2+2I-+2H2O=Mn2++I2+4OH- |
| D.向偏铝酸钠溶液中通入过量的CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
下列有关氯及其化合物叙述错误的是
| A.红热的铜丝在氯气中剧烈燃烧,生成棕黄色的烟 |
| B.大量氯气泄漏时,应用浸有弱碱性溶液的毛巾捂住口鼻身向高处跑 |
| C.AlCl3、FeCl2、FeCl3均可通过化合反应制得 |
| D.向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO |
右表所示的五种元素中,W、X、Y、Z为短周期元素,W元素的核电荷数为X元素的2倍。下列说法错误的是
| |
X |
Y |
|
| W |
|
|
Z |
| T |
|
|
|
A.气态氢化物稳定性:Z > W
B.简单离子半径:X < Y
C.液态WZ4气化需克服分子间作用力
D.根据元素周期律,可以推测T元素的单质具有半导体特性
下列现象或事实可以用同一原理解释的是
| A.浓硫酸和浓盐酸长期露置在空气中浓度均降低 |
| B.氯化铵和碘都可以用加热的方法进行提纯 |
| C.氯水、SO2均能使品红溶液褪色 |
| D.溴蒸汽和NO2气体都能使湿润的淀粉碘化钾试纸变蓝 |
根据下表的信息判断,下列说法错误的是
| 序号 |
反应物 |
产物 |
| ① |
Cl2 、 H2O2 |
Cl- |
| ② |
Cl2、FeI2 |
FeCl2、I2 |
| ③ |
KClO3、HCl |
Cl2、KCl 、H2O |
A.第①组反应的氧化产物为O2
B.第②组反应中Cl2和FeI2的物质的量之比小于或等于1:1
C.第③组反应中生成1molCl2转移6mol电子
D.氧化性由强到弱的顺序为ClO3->Cl2 >I2
已知下列转化关系中,甲、乙均为单质,下列判断正确的是
甲+乙 丙
丙 丙溶液
丙溶液 甲+乙
甲+乙
| A.甲可能是钠 | B.乙可能是氢气 |
| C.丙可能是氧化铝 | D.丙可能是三氧化硫 |
探究铜和浓硫酸的反应,下列装置或操作错误的是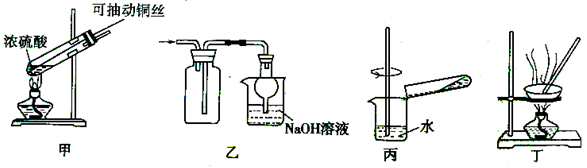
| A.上下移动装置甲中的铜丝可控制生成SO2的量 |
| B.装置乙可用于收集SO2气体 |
| C.为确认CuSO4生成,将试管中的液体倒入装置丙中稀释,观察颜色 |
| D.利用装置丁将硫酸铜溶液加热浓缩、冷却结晶,可析出CuSO4 .5H2O |
下列各组离子在指定溶液中一定能大量共存的是
| A.无色溶液中:Al3+ 、NH4+ 、Cl- 、HS- |
| B.水电离出的C(H+)=1×10-13 mol.L-1的溶液中:Ca2+ 、HCO3- 、I- 、NO3- |
| C.弱酸性溶液中:Na+ 、NH4+ 、HSO3- 、Cl- |
| D.漂白粉的水溶液中:Fe2+ 、SO42-、 Mg2+、 Na+ |
利用右图所示的装置进行下列实验,预测的现象和实际相符的是
| 选项 |
①中的物质 |
②中的物质 |
③中的物质 |
预测③中的现象 |
 |
| A |
浓氨水 |
NaOH |
AlCl3溶液 |
先产生白色沉淀,后沉淀溶解 |
|
| B |
浓盐酸 |
MnO2 |
KI溶液 |
溶液变蓝色 |
|
| C |
浓硫酸 |
Na2SO4 |
Ba(NO3)2溶液 |
无沉淀生成 |
|
| D |
浓硝酸 |
Cu |
含酚酞的NaOH溶液 |
溶液红色褪去 |
某矿物X由Al2O3、Fe2O3、Cu2O、SiO2中的一种或几种物质组成。现进行如图所示实验:
(已知:Cu2O+2H+=Cu+Cu2++H2O)
| A.步骤1中减少的固体一定是混合物 |
B.根据上述步骤可以判断矿物X中 < 1 < 1 |
| C.根据步骤2可以得出蓝色溶液中n(Cu2+)=0.02mol |
| D.根据步骤1、2可以判断出X中氧化铁的质量分数为50% |
运用元素周期律研究元素及其化合物的性质具有重要的意义。
I.部分短周期主族元素的最高价氧化物对应的水化物(浓度均为0.01mol.L-1)溶液的PH和原子序数的关系如下图所示。

(1)元素R在周期表中的位置是 。
(2)元素Y和W形成的Y2W2型化合物中含有化学键的类型为 。
(3)测定Z元素最高价氧化物对应水化物溶液物质的量浓度的方法为 。
II.短周期元素C、O、S能形成多种化合物,如CO2、CS2、COS等
(1)下列能说明碳、硫两种元素非金属性相对强弱的是 (填序号)
A.相同条件下水溶液的PH:Na2CO3 >Na2SO4
B.酸性:H2SO3 >H2CO3
C.CS2中碳元素为+4价,硫元素为-2价
(2)羰基硫(COS)可作为一种熏蒸剂,能防止某些昆虫、线虫的危害,其分子结构和CO2相似
①羰基硫(COS)的电子式为: 。
②羰基硫(COS)用氢氧化钠溶液处理及利用的过程如下:

已知A是一种正盐,则A的化学式为 ;若气体a为单质,反应 II的离子方程式为 。
某溶液A中可能含有NH4+、Fe3+、Al3+、Fe2+、CO32-、NO3-、Cl-、SO42-中的几种离子,且溶液中各离子的物质的量浓度均为0.1mol.L-1。现取该溶液进行如下实验:

(1)溶液A中一定不存在的离子为 (填离子符号)。
(2)溶液A中加入(NH4)2CO3,生成白色沉淀甲和气体甲的原因是 。
(3)白色沉淀乙的成分为 (填化学式)。
(4)为了进一步确定溶液A中是否含有NH4+,另取10ml该溶液,向其中滴加NaOH溶液,沉淀的物质的量随NaOH溶液体积的变化如图所示。

据图回答:
①溶液A中 (填“含有”或“不含有”)NH4+
②所加NaOH溶液的物质的量浓度为 mol.L-1
③若在A溶液中改加10ml0.2mol.L-1Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为 mol
过氧化钙是一种温和的氧化剂,常温下为白色的固体,易溶于酸,难溶于水、乙醇等溶剂。某实验小组拟选用如下装置(部分固定装置略)制备过氧化钙。

(1)请选择必要的装置,按气流方向连接顺序为 (填仪器接口的字母编号,装置可重 复使用)。
(2)根据完整的实验装置进行实验,实验步骤如下:①检验装置的气密性后,装入药品;②打开分液漏斗活塞,通入一段时间气体,加热药品;③反应结束后, (填操作);④拆除装置,取出产物。
(3)利用反应Ca2++H2O2+2NH3+8H2O=CaO2 .8H2O↓+2NH4+,在碱性环境下制取CaO2的装置如下:

①装置A中发生反应的化学方程式为 。
②NH3在Ca2+和H2O2的反应历程中所起的作用是 。
③反应结束后,经 (填操作名称)、洗涤、低温烘干可获得CaO2 .8H2O。
检验CaO2 .8H2O是否洗涤干净的操作为 。
④已知CaO2 在350℃迅速分解生成CaO和O2。若所取产品质量是mg,加热至恒重时,
剩余固体ng,则产品中CaO2 的质量分数为 (用字母表示)。
(4)钙在空气中燃烧生成氮化钙(Ca3N2),同时可能生成过氧化钙。请利用下列试剂,设计试验检验钙的燃烧 产物中是否含有过氧化钙 。(简要说明实验步骤、现象和结论)
限选试剂:酸化的FeCl2溶液、NaOH溶液、KSCN溶液、稀硝酸
草酸镍晶体(NiC2O4 . 2H2O)常用于制镍催化剂。工业上利用镍废渣(主要含镍,还含有Al2O3、Fe、SiO2、CaO等)提取草酸镍晶体的流程如下:

(1)镍废渣粉碎的目的为 。
(2)除铁时,控制不同的条件可以得到不同的滤渣2。已知滤渣2的成分与温度、PH的关系如图所示:

①若控制温度20℃、PH=5,则滤渣2的主要成分为 (填化学式)。
②若控制温度80℃、PH=4,写出该条件下发生反应的离子方程式: 。
(3)滤渣3的主要成分为 (填化学式)。
(4)沉镍时,判断Ni2+是否沉淀完全的方法是 。
(5)硫酸镍(NiSO4)用于化学镀镍时,常用甲醛做还原剂,若氧化产物为CO2,则氧化剂与还原剂的物质的量之比为 。
(6)实验:
I.称量28.7g镀镍试剂,配成100ml溶液;
II.准确量取10.00ml溶液,用0.40mol.l-1的EDTA(Na2H2Y2)标准溶液滴定其中的Ni2+
(离子方程式为Ni2++H2Y2-=NiY2-+2H+),消耗EDTA标准溶液25.00ml;
①配制100ml的镀镍试剂时,需要的仪器除托盘天平、玻璃棒、烧杯、量筒、胶头滴管外,还需要 。
②该镀镍试剂的化学式为 。