生产、生活中的下列现象,主要发生物理变化的是
| A.面团发酵 | B.燃煤供暖 | C.铁窗生锈 | D.海水晒盐 |
空气的成分中,体积分数最大的是
| A.氮气 | B.氧气 | C.稀有气体 | D.二氧化碳 |
“低碳生活”深入人心。倡导“低碳生活”的主要目的是
| A.抑制臭氧层破环 | B.抑制酸雨发生 |
| C.抑制温室效应 | D.抑制土地沙化 |
水净化过程常用到以下消毒剂,其中属于氧化物的是
| A.氯气(Cl2) | B.臭氧(O3) |
| C.次氯酸钙[Ca(ClO)2] | D.二氧化氯(ClO2) |
下图中的符号表示2个氢分子的是 
下列有关氧气性质的描述中,错误的是
| A.氧气不易溶于水 | B.相同条件下,氧气的密度比空气大 |
| C.液态氧无色、无味 | D.氧气能助燃 |
碳元素与氧元素的本质区别是
| A.电子数不同 | B.质子数不同 |
| C.中子数不同 | D.最外层电子数不同 |
下列物质中,不属于大气污染物是
| A.SO2 | B.CO2 | C.NO2 | D.CO |
下列实验操作中,正确的是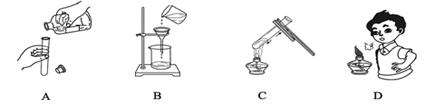
北京是极度缺水的城市。作为北京市民,下列生活习惯应该摒弃的是
| A.用“长流水”洗脸 | B.洗衣服的水用来冲厕所 |
| C.用喝剩下的茶水浇花 | D.用洗过菜的清水擦地 |
地壳中含量最多的元素是
| A.氧 | B.硅 | C.铝 | D.铁 |
加油站无需张贴的图标是
下列反应中,既是氧化反应,又是化合反应的是
| A.用高锰酸钾制氧气 | B.酒精(C2H5OH)在空气中燃烧 |
| C.生石灰变成熟石灰 | D.木炭在氧气中燃烧 |
下列有关物质用途的描述中,错误的是
| A.氢气作清洁燃料 | B.氮气用作焊接金属的保护气 |
| C.O2做气体燃料 | D.稀有气体用于制作霓虹灯 |
下列化学方程式,书写正确的是
A.3Fe+2O2 Fe3O4 Fe3O4 |
B.2HgO 2Hg+ O2 2Hg+ O2 |
C.H2O2 H2↑ + O2↑ H2↑ + O2↑ |
D.4P+5O2 2P2O5 2P2O5 |
下列物质在氧气中燃烧,产生大量白烟的是
| A.木炭 | B.铁丝 | C.石蜡 | D.红磷 |
下列自救措施中,不合理的是
| A.室内起火,不要急于打开所有门窗 |
| B.厨房燃气泄漏,不要立即打开抽油烟机 |
| C.在山林中遇到火灾时,向顺风方向奔跑,脱离火区 |
| D.火灾发生且烟雾较浓时,用湿毛巾捂住口鼻,迅速逃离 |
铀-235可用作核能发电的燃料。其原子核内有92个质子和143个中子。关于铀——235,下列说法错误的是
| A.原子核外有92个电子 | B.原子核外电子数为143 |
| C.相对原子质量为235 | D.铀属于金属元素 |
X是一种杀菌效率高、二次污染小的水处理剂。制备原理为:
2KClO3+4HCl(浓)= 2KCl+2X+Cl2+2H2O,试推断X的化学式为
| A.ClO2 | B.HClO | C.Cl2O5 | D.HClO3 |
下列有关物质性质的描述,属于化学性质的是
| A.浓盐酸易挥发 | B.氯化钠易溶于水 |
| C.铁粉能被磁铁吸引 | D.浓H2SO4具有腐蚀性 |
下列现象或事实,用分子、原子的相关知识加以解释,其中不正确的是
| |
现象或事实 |
解释 |
| A |
稀有气体化学性质稳定 |
最外层电子达到相对稳定结构 |
| B |
氧气和臭氧(O3)化学性质不相同 |
构成物质的分子不同 |
| C |
物质热胀冷缩 |
分子大小随温度改变而改变 |
| D |
水通电分解 |
在化学变化中分子可以再分 |
向盛有氧气和二氧化碳的集气瓶中分别进行下列操作,不能将他们区别开的是
| A.倒入澄清石灰水 | B.伸入燃着的木条 |
| C.伸入带火星的木条 | D.倒入水 |
汽车尾气的排放对环境的污染日益严重。利用四氧化三钴纳米棒作催化剂的催化净化装置,可将汽车尾气中的CO在低温下转化为CO2,过程如下图所示。下列说法正确的是
| A.该催化净化装置能将有毒尾气全部吸收 |
| B.反应前后氧原子个数发生了变化 |
| C.该过程不能说明CO具有可燃性 |
| D.四氧化三钴不参加该化学反应 |
探究二氧化碳通入紫色石蕊试液变红的原因。制作几个用紫色石蕊浸泡的纸花,设计如下实验:①向纸花上喷洒白醋; ②向纸花上滴水;③将纸花烘干并放入干燥的二氧化碳中; ④将纸花放入二氧化碳中。其中必须进行的实验是
| A.②③ | B.③④ | C.②③④ | D.①②③④ |
加热一定量高锰酸钾制氧气,下图所示的有关数量关系,与反应事实不相符的是
生活中处处有化学。
(1) 漂白粉的有效成分是次氯酸钙[Ca(ClO)2],次氯酸钙中氯元素的化合价为 。
(2)干冰可用于人工降雨,主要是因为 。
(3)①右表为“新盖中盖”产品的部分说明。
①该产品的保健功能是“补钙”,这里的“钙”是指 (填字母序号)。
| A.钙原子 | B.钙元素 | C.碳酸钙 | D.钙单质 |
②根据说明计算,每片高钙片中含碳酸钙的质量分数是
(4)热水壶中沉积的水垢主要成分为氢氧化镁和碳酸钙,用食醋(含醋酸CH3COOH)可以除去水垢,其中与氢氧化镁反应的化学方程式为:2CH3COOH+Mg(OH)2 =(CH3COO)2 Mg +2 H2O,则醋酸与碳酸钙反应的化学方程式为 。
宏观与微观相结合是化学学科的思维特点。
(1)在氯化氢、铜和氯化钠3种物质中,由分子构成的是 。
(2)右图为乙醇分子的结构模型,下列说法正确的是 (填字母序号)
| A.乙醇由碳、氢、氧三种元素组成 |
| B.乙醇中含两个碳原子 |
| C.乙醇中碳元素的质量分数最大 |
| D.乙醇中碳、氢、氧三种元素的质量比为2:6:1 |
(3)钙元素的原子结构示意图和在元素周期表中的信息如图所示。甲图中x的数值是 ,y的数值是 ,由此推测钙元素原子在化学变化中易 (填“得电子”或“失电子)。
溶液是生活中常用的混合物。
(1)硫酸铜溶液可用于游泳池消毒,硫酸铜溶液中的溶质是 。
(2)市售的过氧乙酸(CH3COOOH)溶液中溶质的质量分数大多为40%,稳定性差,室温下就可分解成乙酸(CH3COOH),并释放出氧气,该反应的化学方程式为 。将40% 的过氧乙酸溶液稀释成2%,可用于空气消毒, 稀释过程中浓溶液与所加水的质量比为 。
(3)甲、乙两种固体物质的溶解度曲线如图2所示。20 oC时,将等质量的甲、乙分别放入盛有100g水的烧杯中,充分搅拌并升温至50 oC时,实验现象如图1所示。请结合图示回答下列问题:
①曲线N表示 (填“甲”或“乙”)的溶解度随温度变化的情况。
②图1所示的四种溶液中,溶质质量分数最小的是 (填字母序号,下同),一定不饱和的是 。
化学是研究物质的组成、结构、性质及变化规律的科学。化学课外小组的同学利用下图所示装置对水进行研究。
(1)将天然水倒入图A所示的蒸发皿中,观察到蒸发皿底部有一道一道的“水痕”,这说明天然水是 (填物质类别)。
(2)用如图B所示的装置对天然水进行净化,其中小卵石、石英砂、膨松棉的作用是 。
(3)向图C的烧杯中倒入蒸馏水,观察到 ,该反应的化学方程式为 ,利用生石灰的这一性质,除制取熟石灰外,还可以 。
(4)利用D图可以研究水分子的构成,与试管1连接的是电源的 极,要推测水分子的构成,仅需下列条件中 (填数字序号)就可以达到目的。
①两级生成气体的体积比 ②氢分子的构成
③氧分子的构成 ④气体体积比与分子个数比的关系
⑤生成氢气和氧气的质量比
A、B、C、D是初中化学中的常见物质,有如图1所示的转化关系(反应条件、部分反应物及产物已略去):
(1)若A是大理石的主要成分,写出下列反应的化学方程式:A→B ,D→A 。
(2)若A是人体含量最多的物质,则B→D 化学方程式为 。
(3)取上述物质中的两种,用如图2所示的装置进行实验,观察到U型管中液面发生偏转,该过程集气瓶内可能观察到的现象是 。
下图为实验室制取气体的常用装置,根据图示回答问题。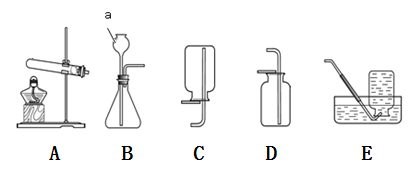
(1)仪器a的名称是 。
(2)用高锰酸钾制取氧气的化学方程式是 ,选用的发生装置是 。
(3)二氧化碳只能用向上排空气法收集,验满的方法是 。
(4)锌放入稀硫酸中能产生氢气,实验室用该反应制取氢气。则制取并收集氢气可选用的装置是 。
水在化学实验中的作用不可忽视,下图中六个实验分别用到水。请结合图示回答下列问题:
 (1)A实验在集气瓶中预先装入少量水的目的是 。
(1)A实验在集气瓶中预先装入少量水的目的是 。
(2)用排水法收集气体时,一方面能观察到气体是否集满,另一方面水可以_______。
(3)粗盐提纯时,水的作用是 。
(4)实验D中水的作用是提供热量和 。
(5)实验E中的水是 。
(6)在F实验中,集气瓶内预先装入少量水,可以起到的作用有 。
在研究氧气的性质时,同学们发现含氧元素的质量可以相互转化,如“氧化物甲 氧气
氧气 氧化物甲”的转化,反应I的化学方程式为 。
氧化物甲”的转化,反应I的化学方程式为 。
【提出问题】铁丝能在氧气中燃烧,观察到火星四射、剧烈燃烧 。能不能将燃烧产物四氧化三铁再转化为铁单质呢?
【查阅资料】(1)Fe3O4的分解温度为1538 oC
(2)CO具有还原性,能将某些金属氧化物还原为金属单质
(3)酒精灯外焰温度约700 oC,酒精喷灯火焰温度约1000 oC
(4)铁丝为银白色,铁粉为黑色
【设计实验】同学们设计了如下图所示的实验装置,对CO能不能将四氧化三铁转化为铁进行探究。结合图示回答问题。
(1)B装置中浓硫酸具有吸水性,能除去二氧化碳中的水蒸气,浓硫酸吸水过程会 (填“吸热”或“放热”)。
(2)C装置可将二氧化碳转化为一氧化碳,反应的化学方程式为 。
(3)F处点燃酒精的目的是 。
(4)依据现象得出结论,该设计中观察到以下现象,其中可以说明四氧化三铁与一氧化碳发生反应的现象是 (填字母序号)。
| A.澄清石灰水变浑浊 | B.反应前后D中质量减轻 |
| C.F导管口有蓝色火焰 | D.加热时,四氧化三铁变红 |
【反思与评价】由于上述实验设计有明显不足,致使某些现象不能作为推理的依据,其中的不足是 。
(3分)在科学家眼里,二氧化碳是可以利用的重要资源。在一定条件下,二氧化碳和金属钠反应可以制金刚石,反应的化学方程式为CO2+4Na C(金刚石)+2Na2O。请计算46 g金属钠理论上可制得金刚石的质量。
C(金刚石)+2Na2O。请计算46 g金属钠理论上可制得金刚石的质量。
某造纸厂排放的废水中含有Na2CO3和NaOH。为了测定废水中Na2CO3的质量分数,取废水150g,逐滴加入稀盐酸至过量,测得生成气体质量与所加稀盐酸质量关系如下图所示(提示:NaOH+HCl=NaCl+H2O,Na2CO3 + 2HCl =" 2NaCl" + H2O + CO2↑) 。该废水中Na2CO3的质量分数和所用稀盐酸中溶质的质量分数分别是多少?