氧化还原反应在生产、生活中具有广泛的用途。下列生产、生活中的事例不属于氧化还原反应的是( )
| A.金属冶炼 | B.燃放鞭炮 | C.食物腐败 | D.点制豆腐 |
能正确表示下列反应的离子方程式的是
| A.将少量二氧化硫通入次氯酸钠溶液中:SO2+H2O+ClO-=SO42-+Cl-+2H+ |
| B.向氯化铁溶液中滴加HI溶液:2Fe3+ +2HI=2Fe2++2H++I2 |
| C.硝酸铝溶液中加入过量氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O |
| D.向NaHSO4溶液中滴入Ba(OH)2溶液至SO42—恰好转化为沉淀:H++SO42-+Ba2++OH-=BaSO4↓+H2O |
分子式为C5H10O2的酯,且有2个甲基的同分异构体共有(不考虑立体异构)
| A.3种 | B.4种 | C.5种 | D.6种 |
下列过程没有发生化学反应的是
| A.利用氢氟酸刻蚀玻璃 |
| B.焰色反应 |
| C.酒精消毒杀菌 |
| D.利用油脂制取肥皂 |
恒温恒容下,向2L密闭容器中加入MgSO4(s)和CO(g),发生反应:
MgSO4(s)+CO(g) MgO(s)+CO2(g)+SO2(g),反应过程中测定的部分数据见下表:
MgO(s)+CO2(g)+SO2(g),反应过程中测定的部分数据见下表:
| 反应时间/min |
n(MgSO4)/mol |
n(CO)/mol[ |
n(CO2) / mol |
| 0 |
3.00 |
2.00 |
0 |
| 2 |
0.80 |
||
| 4 |
1.20 |
下列说法正确的是
A.反应在0~2min内的平均速率为v(SO2)=0.6 mol·L-1·min-1
B.反应在2~4min内容器内压强恒定不变
C.若升高温度,反应的平衡常数变为1.1,则正反应为吸热反应
D.保持其他条件不变,起始时向容器中充入1.00mol MgSO4和1.00molCO,到达平衡时n(CO2)<0.60mol
常温下,向10 mL 0.1 mol·L-1的H2C2O4溶液中逐滴加入0.1 mol·L-1 KOH溶液,所得滴定曲线如图所示。下列说法正确的是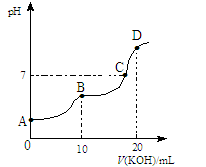
| A.KHC2O4溶液呈弱碱性 |
| B.B点时:c(K+)>c(HC2O4-)>c(H+)>c(OH-) |
| C.C点时:c(HC2O4-)+c(C2O42-)+c(H2C2O4)<c(K+)<c(HC2O4-)+2c(C2O42-)+c(H2C2O4) |
| D.D点时:c(H+)+ c(HC2O4-)+ c(H2C2O4)= c(OH-) |