在硫酸铝、硫酸钾和明矾的混合溶液中,如果c(SO42-)="0.2" mol/L,当加入等体积、某浓度的KOH溶液时,恰好沉淀完全,则所得溶液中K + 的物质的量浓度是( )
| A.0.2 mol/L | B.0.25 mol/L | C.0.1 mol/L | D.0.225 mol/L |
X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15;X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76 g•L-1;W的质子数是X、Y、Z、M四种元素质子数之和的1/2 。下列说法正确的是
| A.XZ2、X2M2、M2Z2均为直线型的共价化合物 |
| B.由X元素形成的单质不一定是原子晶体 |
| C.原子半径:Z>Y>X |
| D.由Z、W两种元素形成的化合物一定既有离子键,又有共价键 |
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知
| A.Y元素氧化物对应水化物的酸性一定弱于Z |
| B.W、X、Y中最简单氢化物稳定性最强的是X |
| C.X元素形成的单核阴离子还原性大于Y |
| D.Z元素单质在化学反应中只表现氧化性 |
下列说法正确的是
| A.(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-=Fe(OH)2↓ |
B.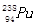 与 与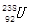 互为同位素 互为同位素 |
| C.H3O+和NH4+具有的电子数相同 |
| D.用BaCl2溶液鉴别AgNO3溶液和K2SO4溶液 |
下列物质中均含有酸性杂质,除去这些杂质的方法中正确的是
| A.乙醇中含乙酸杂质:加入足量氧化钙,蒸馏 |
| B.制氯气时,依次通过饱和NaHCO3溶液和浓硫酸净化气体 |
| C.CO2中混有H2S通过足量的浓硫酸溶液洗气,以得到纯净的CO2 |
| D.通过灼热的镁粉除去N2中的O2 |
下列实验操作能达到目的的是
| A.用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液 |
| B.制取二氧化氮时,用水或NaOH溶液吸收尾气 |
| C.为测定Na2CO3和NaHCO3混合物中Na2CO3质量分数,取a g混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b g,该方案可行。 |
| D.为测定镀锌铁皮的锌层厚度,将镀锌铁皮与足量盐酸反应待气泡明显减少时取出,洗涤,烘干,称重。若烘干时间过长,会导致测定结果偏小。 |