研究发现,空气中少量的能参与硫酸型酸雨的形成,反应过程如下:
① ② ③
在上述过程中的作用,与在下述变化中的作用相似的是()
| A. | 潮湿的氯气通过盛有浓 的洗气瓶 | B. | 硫化氢通入浓 |
| C. | 浓 滴入萤石中,加热 | D. | 加入少量的 使乙酸乙酯水解 |
2007年诺贝尔化学奖授予德国化学家格哈德·埃特尔,以表彰他在界面化学研究领域取得的成就。下面实例中涉及到的变化都属于“界面化学”的范畴。其中正确的是
| A.在汽车上安装催化转化器,使一氧化碳在催化剂表面氧化为二氧化碳,可减少一氧化碳的排放 |
| B.泄漏在海洋中的原油可被海洋生物迅速分解而除去 |
| C.铁生锈是铁与空气中的氧气、水蒸气直接化合生成了水合氧化铁(Fe2O3、nH2O)的结果 |
| D.放置在空气中澄清石灰水表面出现的白色固体的主要成分是氢氧化钙 |
通式为C6H5—R(R为-H、-C2H5、-OH、-SO3H、-NO2和–COOH)的6种有有机物,取等质量的6种物质分别混合于乙醚中,然后用苛性钠溶液进行萃取,振荡一段时间后,静置,能进入水层的物质有()
| A.1种 | B.2种 | C.3种 | D.4种 |
下列装置或操作能达到实验目的(必要的夹持装置及石棉网已省略)的是()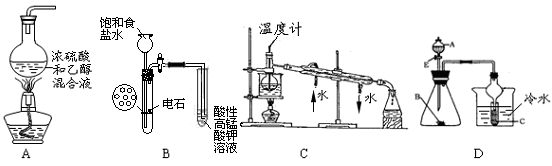
| A.实验室制乙烯 | B.实验室制乙炔并验证乙炔发生氧化反应 |
| C.实验室中分馏石油 | |
| D.若A为醋酸,B为贝壳(粉状),C为苯酚钠溶液,验证醋酸、苯酚、碳酸酸性的强弱(不考虑醋酸的挥发) |
难溶于水而且比水轻的含氧有机物是()
①硝基苯②甲苯③ 溴苯④植物油⑤蚁醛⑥乙酸乙酯⑦硬脂酸甘油酯
溴苯④植物油⑤蚁醛⑥乙酸乙酯⑦硬脂酸甘油酯
| A.②④⑥⑦ | B.①②④⑤ | C.④⑥⑦ | D.①②③ |
甘氨酸和丙氨酸混合,在一定条件下,发生缩合反应生成二肽化合物共有( )
| A.5种 | B.4种 | C.3种 | D.2种 |