下面有三则关于“CO2”的消息:
(1)1999年美国《科学》杂志报道:在40Gpa的高压下,用激光器加热到1800K,人们成功地制得了原子晶体干冰。
(2)CCTV《科技博览》报道,2004年3月中科院首创用CO2合成降解塑料聚二氧化碳。
(3)超临界流体是温度和压力同时高于临界值的流体,也即压缩到具有接近液体密度的气体,是物质介于气态和液态之间的一种新的状态。
针对以上消息,下列推断中正确的是
①原子晶体干冰有很高的熔点、沸点;②原子晶体干冰易汽化,可用作致冷剂;③原子晶体干冰的硬度大,可用作耐磨材料;④聚二氧化碳塑料是通过加聚反应得到的;⑤聚二氧化碳塑料与干冰互为同素异形体;⑥聚二氧化碳塑料都属于纯净物;⑦聚二氧化碳塑料的使用会产生白色污染;⑧超临界二氧化碳与CO2的物理性质不同,但化学性质相同;⑨超临界二氧化碳可能是一种原子晶体;⑩超临界二氧化碳代替氟利昂可减轻对臭氧层的破坏
| A.②③④⑨⑩ | B.②③④⑤⑥⑧⑩ | C.①③④⑧⑩ | D.③④⑦⑧⑨ |
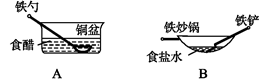
下列有关实验装置及用途叙述完全正确的是

| A.a装置检验消去产物,中间应加水洗装置 | B.b装置检验酸性:盐酸>碳酸>苯酚 |
| C.c装置用于实验室制取并收集乙烯 | D.d装置用于实验室制硝基苯 |
莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中。下列关于这两种有机化合物(见下图)的说法正确的是
| A.两种酸都能与溴水发生反应 |
| B.鞣酸分子与莽草酸分子相比多了两个碳碳双键 |
| C.1mol莽草酸完全燃烧消耗7molO2 |
| D.等物质的量的两种酸与足量氢氧化钠反应,消耗氢氧化钠的量相同 |
下列根据事实所作出的结论正确的是
| 事实 |
结论 |
| A.完全燃烧产物是CO2和H2O的物质 |
一定只含C、H元素 |
| B.灼烧棉织品、羊毛衫和涤纶衣物 |
有烧焦羽毛气味的是羊毛衫 |
| C.在淀粉溶液中加入市售的加碘食盐不出现蓝色 |
不能说明此盐不含碘 |
| D.甲乙两种物质,相对分子质量相同,结构不同 |
甲和乙一定是同分异构体 |
下列说法正确的是
| A.麦芽糖的水解产物能发生银镜反应 |
| B.四氟乙烯(CF2=CF2)中所有的原子都在同一个平面上 |
C.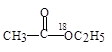 在酸性条件下水解产物是 在酸性条件下水解产物是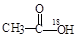 和 和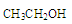 |
| D.淀粉溶液加适量浓硫酸加热一会儿后,滴入银氨溶液无银镜生成,说明淀粉未水解 |
相同材质的铁在下图中的四种情况下最不易被腐蚀的是