现有部分前四周期元素的性质或原子结构如下表:
| 元素编号 |
元素性质或原子结构 |
| A |
第三周期中的半导体材料 |
| B |
L层s电子数比p电子数少1 |
| C |
第三周期主族元素中其第一电离能最大 |
| D |
前四周期呀中其未成对电子数最多 |
(1)B单质分子中,含有________个 键和__________个
键和__________个 键,元素B的气态氢化物的空间型为________________。
键,元素B的气态氢化物的空间型为________________。
(2)C单质的熔点____________A单质的熔点(填“高于”或“低于”),其原因是:_______________
(3)写出元素D基态原子的电子排布式:______________________。
下表为短周期的一部分,推断关于Y、Z、M的说法正确的是
| A.非金属性:Y >Z>M | B.原子半径:M>Z>Y |
| C.气态氢化物的稳定性:Y<M<Z | D.ZM2分子中各原子的最外层均满足8e-稳定结构 |
下列溶液中各微粒的浓度关系不正确的是
| A.0.1 mol/L的HCOOH溶液中:c(HCOO—)+c(OH—)=c(H+) |
| B.1 L 0.1 mol/L的CuSO4·(NH4)2SO4·6H2O的溶液中: c(SO42—)>c(NH4+)>c(Cu2+)>c(H+)>c (OH—) |
| C.0.1 mol/L 的NaHCO3溶液中: c(Na+)+c(H+)=c(HCO3—)+2c(CO32—)+c(OH—) |
| D.等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液中: |
c(Na+)>c(HX)>c(X—)>c(H+)>c(OH—)
根据实验目的判断下列实验操作或装置正确的是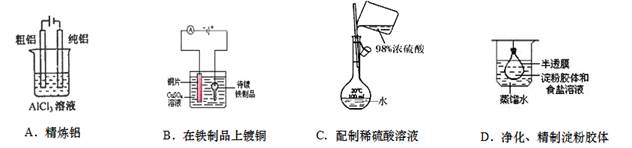
关于反应中的先后顺序,下列评价正确的是
| A.向浓度都为0.1 mol/L的FeCl3和CuCl2混合溶液中加入铁粉,CuCl2首先反应 |
| B.向NH4Al(SO4)2溶液中滴加少量的NaOH溶液,NH4+首先反应 |
| C.向浓度都为0.1 mol/LNa2 CO3和NaOH溶液通入CO2气体,NaOH首先反应 |
| D.向浓度都为0.1 mol/L的FeCl3加入质量相同、颗粒大小相同的铁和铜,铜首先反应 |
常温下,下列各组离子在溶液中一定能大量共存的是
| A.pH=12的溶液:K+、Na+、CH3COO—、CO32— |
| B.与铝反应产生大量氢气的溶液:Mg2+、K+、HCO3—、NO3— |
| C.由水电离产生的c(H+)=10-13mol/L的溶液:NH4+、Ca2+、SO32—、Cl— |
| D.0.1 mol/L的NaNO3溶液:H+、Fe2+、Cl—、SO42— |