在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K与温度t的关系如下:
CO(g)+H2O(g),其化学平衡常数K与温度t的关系如下:
| T/℃ |
700 |
800 |
830 |
1000 |
1200 |
| K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
请回答下列问题:
(1)该反应的化学平衡常数表达式K= 。
(2)该反应为 反应。(填“吸热”或“放热”)
(3)800℃时,固定容积的密闭容器中放入混合物,起始浓度为c(CO)=0.01 mol·L-1,c(H2O)=0.03 mol·L-1,c(CO2)=0.01 mol·L-1,c(H2)=0.05 mol·L-1,则反应开始时,H2O的消耗速率比生成速率 (填“大”、“小”或“不能确定”)
(4)830℃时,在1L的固定容积的密闭容器中放入2mol CO2和1mol H2,平衡后CO2的转化率为 ,H2的转化率为 。
已知一定温度和压强下,在容积为VL的密闭容器中充入1mol A和1mol B,保持恒温恒压下反应:A(g) + B(g)  C(g),△H<0。达到平衡时,C的体积分数为40%。试回答有关问题:
C(g),△H<0。达到平衡时,C的体积分数为40%。试回答有关问题:
(1)升温时,C的反应速率_______(填“加快”、“减慢”或“不变”)
(2)若平衡时,保持容器容积不变,使容器内压强增大,则平衡_______
| A.一定向正反应方向移动 | B.一定向逆反应方向移动 |
| C.一定不移动 | D.不一定移动 |
(3)若使温度、压强在上述条件下恒定不变,在密闭容器中充入2mol A和2 mol B,则反应达到平衡时,C的体积分数为_____;容器的容积为____(请写出计算过程)
1840年盖斯指出:若是一个反应可以分几步进行,则各步反应的反应热总和与这个反应一次发生时的反应热相同。请回答:
(1)已知热化学方程式:C(S,金刚石)+ O2(g)= CO2(g) △H = -395.41KJ/mol
C(S,石墨)+ O2(g)= CO2(g) △H = -393.51KJ/mol
则金刚石转化为石墨的热化学方程式为____________________,由热化学方程式看来更稳定的碳的同素异形体是____________________
(2)燃烧3.1g白磷比燃烧3.1g红磷放出的热量多1.839KJ,则白磷转化为红磷的热化学方程式是____________________________,相同温度下,能量状态最低的是__________。
已知A的产量通常用来衡量一个国家的石油化工水平,现以A为主要原料合成一种具有果香味的物质E,其合成路线如下图所示。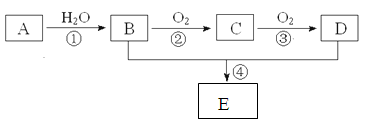
请回答下列问题:
(1)写出A的电子式,B、D分子中的官能团名称分别是 、。
(2)写出下列反应的化学方程式,并注明反应类型:
①,;
②,;
④,。
(12分)现有反应:mA(g)+nB(g) pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)该反应的逆反应为_________热反应,且m +n ________ p(填“>”“=”“<”)。
(2)减压时,A的质量分数_________。(填“增大”“减小”或“不变”,下同)
(3)若加入B(体积不变),则A的转化率__________。
(4)若升高温度,则平衡时B、C的浓度之比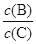 将_________。
将_________。
(5)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色_______ (填“变深”“变浅”或“不变”)。
将等物质的量的H2和I2充入体积为2 L的密闭容器中,进行反应:H2(g)+ I2(g) 2HI(g),测得2min内v (HI)= 0.1 mol•L-1•min-1,2min 后I2(g)的浓度为0.4 mol•L-1,试确定:
2HI(g),测得2min内v (HI)= 0.1 mol•L-1•min-1,2min 后I2(g)的浓度为0.4 mol•L-1,试确定:
(1)2min内以H2所表示的反应速率为___________________;
(2)I2的起始物质的量为___________________;
(3)2min末HI的浓度为___________________