丙烯酸的结构简式为CH2=CH—COOH,其对应的性质不正确的是 ( )
| A.能与钠反应放出氢气 | B.能与新制Cu(OH)2反应 |
| C.能与溴水发生取代反应 | D.能发生加聚反应生成高分子化合物 |
一定温度下,反应2 SO2 + O2 2SO3,达到平衡时,n(SO2):n(O2):n(SO3)=2:3:4。缩小体积,反应再次达到平衡时,n(O2)="0.8mol," n(SO3)=1.4mol,此时SO2的物质的量应是
2SO3,达到平衡时,n(SO2):n(O2):n(SO3)=2:3:4。缩小体积,反应再次达到平衡时,n(O2)="0.8mol," n(SO3)=1.4mol,此时SO2的物质的量应是
| A.0.4mol | B.0.6mol | C.0.8mol | D.1.2mol |
合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:
N2(g)+3H2(g) 2NH3(g),673K,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是
2NH3(g),673K,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是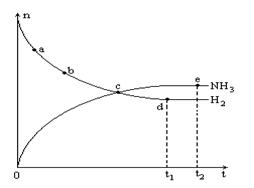
| A.点a的逆反应速率比点b的大 |
| B.点c处反应达到平衡 |
| C.点d (t1时刻)和点e (t2时刻)处n(N2)不一样 |
| D.其他条件不变,773K下反应至t1时刻,n(H2)比上图中d点的值大 |
对达到平衡状态的可逆反应:X+Y 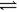 W+Z,在t'时增大压强,则正逆反应速率变化如图所示(V代表速率,t代表时间)下列有关X、Y、Z、W的状态叙述正确的是
W+Z,在t'时增大压强,则正逆反应速率变化如图所示(V代表速率,t代表时间)下列有关X、Y、Z、W的状态叙述正确的是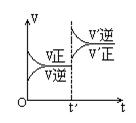
| A.X、Y、W为气体,Z不是气体 |
| B.X、Y为气体,W、Z中有一种是气体 |
| C.W、Z为气体,X、Y中有一种是气体 |
| D.W、Z中有一种为气体,X、Y都不是气体 |
下列各组物质的颜色变化,可用勒夏特列原理解释的是
| A.新制的氯水在光照条件下颜色变浅 |
| B.H2、I2、HI平衡混合气加压后颜色变深 |
| C.KI溶液加氯水振荡后颜色变深 |
| D.加入催化剂有利于氨氧化的反应 |
在密闭容器中,反应xA(g)+yB(g) zC(g),达到平衡后测得A气体的浓度为0.5mol•L—1。保持温度不变,将密闭容器的容积增加一倍,当达到新的平衡时,测得A的浓度为0.3mol•L—1,则下列叙述中正确的是
zC(g),达到平衡后测得A气体的浓度为0.5mol•L—1。保持温度不变,将密闭容器的容积增加一倍,当达到新的平衡时,测得A的浓度为0.3mol•L—1,则下列叙述中正确的是
| A.平衡向正反应方向移动 | B.x+y>z |
| C.物质C的体积分数增大 | D.物质B的转化率增大 |