2007年12月4日浙江省卫生厅公布的最常见的四种疾病中,高血压排在第一位,胆结石
排在第二位,可见在全民社会中普及如何预防胆结石显得尤为重要。从化学上讲,非结合胆红素(VCB)分子有羟基,被氧化后(生成羧基)与钙离子结合形成胆红素钙的反应,就是一个生成沉淀的离子反应,从动态平衡的角度分析能预防胆结石的方法是( )
A.大量食用纯碱可使钙离子沉淀完全,预防胆结石产生
B.不食用含钙的食品
C.适量服用维生素E、维生素C等抗氧化自由基可预防胆结石
D.手术切除胆囊
短周期主族元素A、B、C、D、E的原子序数依次增大,其中A与C同主族,A与其它元素不在同一周期,B与D同主族,常温下D的单质为淡黄色固体。下列推断中正确的是
A.离子半径由小到大的顺序:r(B)<r(C)<r(E)
B.元素B、D分别与A形成的化合物的热稳定性:D>B
C.元素D的氧化物对应水化物的酸性比E的弱
D.元素B与A形成的某种化合物和B与C形成的某种化合物反应,可能包含了离子键与共价键的断裂和形成
化学与社会、社会密切相关,下列说法正确的是
| A.工业上利用二氧化硅在高温条件下与焦炭反应,生成单质硅和二氧化碳的原理,制取粗硅 |
| B.手指不慎被玻璃划伤流血,可向伤口上涂FeCl3溶液,是因为FeCl3溶液可杀菌消毒 |
| C.2014年山东莱芜共出现284天雾霾天气,对煤进行液化和气化等物理变化的处理,可减少雾霾天气的发生 |
| D.白酒放置一定时间香味更浓,是因为白酒中乙醇与少量的有机酸反应生成具有香味的酯 |
一定条件下进行反应:A(g)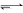 B(g)+C (g),向2.0 L恒容密闭容器中充入1.0 mol A(g),经过一段时间后达到平衡。反应过程中测得的有关数据见下表:
B(g)+C (g),向2.0 L恒容密闭容器中充入1.0 mol A(g),经过一段时间后达到平衡。反应过程中测得的有关数据见下表:
| t/s |
0 |
2 |
4 |
6 |
8 |
| n(B)/mol |
0 |
0.30 |
0.39 |
0.40 |
0.40 |
下列说法正确的是
A.反应前2min的平均速率v(B)="0.15" mol/(L·min)
B.保持其他条件不变,升高温度,平衡时c(B)="0.22" mol·L-1,则反应的ΔH < 0
C.保持其他条件不变,起始向容器中充入2.0 mol A,反应达到平衡时C的体积分数减小
D.保持其他条件不变,起始向容器中充入1.2 mol A、0.60 mol B和0.60 mol C,反应达到平衡前的速率:v(正)<v(逆)
常温下,向20.00 mL 0.1000 mol·L—1 (NH4)2SO4溶液中逐滴加入0.2000 mol·L—1NaOH时,溶液的pH与所加NaOH溶液体积的关系如右下图所示(不考虑挥发)。下列说法正确的是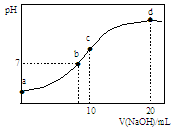
| A.点a所示溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-) |
| B.点b所示溶液中:c(NH4+)=c(Na+)>c(H+)=c(OH-) |
| C.点c所示溶液中:c(SO42-)+ c(H+)= c(NH3·H2O )+ c(OH-) |
| D.点d所示溶液中:c(SO42-)>c(NH3·H2O )>c(OH-)>c(NH4+) |
由一种阳离子和两种酸根离子组成的盐称混盐。下列关于混盐Na4S2O3的有关判断,不正确的是
| A.向溶液中加入酚酞试剂溶液变红,说明该混盐水溶液呈碱性 |
| B.向该混盐加入稀H2SO4产生使品红褪色的气体,说明溶液中含有SO32- |
| C.该混盐在酸性条件下可生成淡黄色固体,说明产物中含有硫单质 |
| D.用玻璃棒蘸取该混盐溶液灼烧,火焰呈黄色,说明溶液中含有Na+ |