已知周期表中,元素Q、R、W、Y与元素X相邻。Y的最高化合价氧化物的水化物是强酸。回答下列问题:







(1)W与Q可以形成一种高温结构陶瓷材料。W的氯化物分子呈正四面体结构,W的氧化物的晶体类型是 ;
(2)Q的具有相同化合价且可以相互转变的氧化物是 ;
(3)R和Y形成的二元化合物中,R呈现最高化合价的化合物的化学式是 ;
(4)这5个元素的氢化物分子中,①立体结构类型相同的氢化物的沸点从高到低排列次序是(填化学式) ,其原因是 ;
②电子总数相同的氢化物的化学式和立体结构分别是
;
(5)W和Q所形成的结构陶瓷材料的一种合成方法如下:W的氯化物与Q的氢化物加热反应,生成化合物W(QH2)4和HCL气体;W(QH2)4在高温下分解生成Q的氢化物和该陶瓷材料。上述相关反应的化学方程式(各物质用化学式表示)是 。
工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁[Fe(OH)SO4]的工艺流程如下: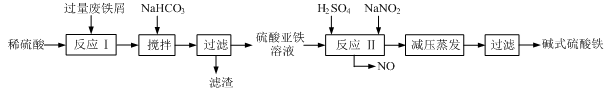
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 |
Fe(OH)3 |
Fe(OH)2 |
Al(OH)3 |
| 开始沉淀 |
2.3 |
7.5 |
3.4 |
| 完全沉淀 |
3.2 |
9.7 |
4.4 |
回答下列问题:
(1)加入过量废铁屑的目的是,此时溶液中存在的阳离子主要有,用NaHCO3调整溶液pH时的离子方程式是。
(2)在实际生产中,反应Ⅱ中常同时通入O2以减少NaNO2的用量,同时通入O2的作用是。
(3)碱式硫酸铁溶于水后能电离产生[Fe(OH)]2+离子,写出[Fe(OH)]2+发生水解反应生成Fe(OH)3的离子方程式。
(4)已知废铁屑中铁元素的质量分数为84.0%,若不考虑每步反应中铁元素的损耗,现有100吨废铁屑理论上最多能生产吨碱式硫酸铁。
工业上以锂辉石(Li2O·Al2O3·4SiO2,含少量Ca、Mg元素)为原料生产碳酸锂。其部分工艺流程如下: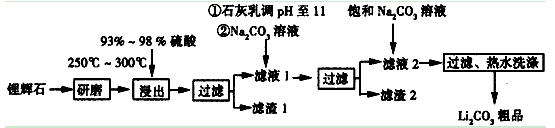
已知:①Li2O·Al2O3·4SiO2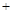 H2SO4(浓)
H2SO4(浓) Li2SO4
Li2SO4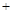 Al2O3·4SiO2·H2O↓
Al2O3·4SiO2·H2O↓
②某些物质的溶解度(S)如下表所示:
| T/℃ |
20 |
40 |
60 |
80 |
 (Li2CO3)/g (Li2CO3)/g |
1.33 |
1.17 |
1.01 |
0.85 |
 (Li2SO4)/g (Li2SO4)/g |
34.2 |
32.8 |
31.9 |
30.7 |
③从滤渣1中提取出Si的部分流程如下图所示:
根据以上信息,请回答下列问题:
(1)括号内应提供的相应条件和物质 、 。
(2)方框中所得物质的化学式 。
(3)使用浓硫酸并加热到250℃~300℃的目的是 。
(4)②处加Na2CO3溶液所发生反应的离子方程式 、 。
(5)滤渣2的主要成分有 。
(6)如何检验Li2CO3是否洗涤干净? 。
某强酸性溶液X中含有Ba2+、Al3+、NH4+、Fe2+、Fe3+、CO32-、SiO32-、SO42-、NO3-中的一种或几种离子。为确定溶液X的成分,进行如下实验: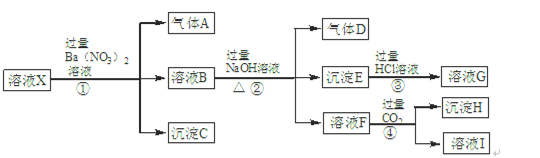
根据以上信息,请回答下列问题:
(1)溶液X中肯定不含有的离子是,不能确定是否含有的离子是,若要确定是否含有这种离子,最可靠方法是:
。
(2)溶液I中所含溶质有(填化学式)。
(3)步骤①②③④中,发生符合“强酸制弱酸”反应的步骤是(填序号)。
(4)步骤①中生成气体A的离子方程式是。
已知:①标准状况下,1体积水中最多能溶解500体积的HCl;
②饱和NaCl溶液的浓度约为5.00 mol·L-1。
在标准状况下,将448LHCl气体溶于1 L水中,所得溶液A的密度为1.20 g·cm-3,则溶液A中HCl的物质的量浓度为。(本题计算结果均取三位有效数字)
(1)若使Cl-浓度与溶液A中的Cl-浓度相等,则在1 L NaCl饱和溶液中还应溶解约L标准状况下HCl气体 (溶液体积变化忽略不计)。
(2)取10.0mL溶液A稀释成500mL溶液B,则溶液B中HCl的物质的量浓度为。
(3)在溶液B的配制过程中,使用前必须检查是否漏液的仪器有;下列配制操作,造成溶液B浓度偏低的是_______________(选填序号)。
a.容量瓶用蒸馏水洗涤后未干燥
b.量取溶液A的量筒用蒸馏水洗涤后未干燥
c.定容时,俯视液面加水至刻度线
d.加水定容时液面不慎超过刻度线,立即用胶头滴管吸出部分水使液面刚好达刻度线
e.烧杯中溶液移入容量瓶后,未用水洗涤烧杯和玻璃棒即定容
亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于工业生产的漂白及消毒。
下图是过氧化氢法生产亚氯酸钠的工艺流程图:
相关物质的性质如下:
① ClO2沸点低易气化;浓度较高的ClO2气体易分解爆炸。
② NaClO2溶解度随温度升高而增大,适当条件下可结晶析出NaClO2·3H2O。
(1).在ClO2发生器中通入SO2的同时鼓入空气,其作用是________(填序号)。
A.将SO2氧化成SO3,增强酸性
B.稀释ClO2以防止爆炸
C.将NaClO3氧化成ClO2
(2)为确保H2O2充分参与反应,吸收塔内温度不宜较高,其原因是______________。
(3)160 g·L-1 NaOH溶液的物质的量浓度为______________,在实验室若要配制450mL该物质的量浓度NaOH溶液,应称取NaOH的质量为__________克。
(4)写出吸收塔内反应的化学方程式_____________________________________。
(5)从滤液中得到NaClO2·3H2O粗晶体的实验操作依次是____________(填序号)。
A.蒸馏 B.蒸发 C.灼烧 D.过滤 E.冷却结晶
要得到更纯的NaClO2·3H2O晶体必须进一步的操作是________(填操作名称)。