NA代表阿伏加德罗常数。下列说法中,不正确的是
| A.标准状况下,NO和 O2各11.2 L混合,所得混合气体的分子总数为 0.75 NA |
| B.25℃时,l L pH=13的Ba(OH)2溶液中含有OH―的数目为0.1 NA |
| C.1 mol C30H62分子中含有共价键的数目为 91 NA |
| D.2.8g乙烯与丙烯的混合物中含碳原子的数目为 0.2NA |
下列有关离子检验的操作和实验结论都正确的是
| 选项 |
实验操作及现象 |
实验结论 |
| A |
向某溶液中加入氯化钡溶液,有白色沉淀生成,再加盐酸酸化,沉淀不溶解 |
该溶液中一定含有SO42— |
| B |
向某溶液中先加入几滴KSCN溶液,再滴入酸性高锰酸钾溶液,溶液变为浅红色 |
该溶液中一定含有Fe2+ |
| C |
在酒精灯上加热铝箔,铝箔熔化,但不滴落,好像有一层膜兜着 |
铝易被氧化;铝的熔点比氧化铝低 |
| D |
向某溶液中加入稀盐酸,产生能使澄清石灰水变浑浊的无色气体 |
该溶液中一定含有CO32— |
下列所述事实与化学(离子)方程式不相符的是
| A.能说明非金属性Cl > C: 2HCl+CaCO3==CaCl2+CO2↑+H2O |
| B.能说明氧化性H2O2 > Fe3+: 2Fe2++H2O2+2H+ ==2Fe3++2H2O |
| C.已知:H+(aq)+OH—(aq)="=H2O(l)" ΔH=-57.3kJ·mol-1(稀溶液),能说明稀硫酸与NaOH稀溶液反应生成1mol水,放出的热量为57.3 kJ |
D.能说明CH3COOH是弱电解质: CH3COO—+H2O 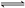 CH3COOH+OH— CH3COOH+OH— |
下列各组离子在指定溶液中能大量共存的是
| A.在80℃pH= 10的溶液中:Na+ 、CH3CHO、Ag(NH3)2+、NO3— |
| B.溶液中能大量共存,通入CO2后仍能大量共存:K+、Ca2+、Cl—、NO3— |
| C.与镁反应只产生氢气的溶液中:NO3—、Cl—、H+、A13+ |
D.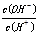 =1.0×10-12溶液中:C6H5O—、K+、SO42—、CH3COO— =1.0×10-12溶液中:C6H5O—、K+、SO42—、CH3COO— |
下列分类图表示的关系完全正确的是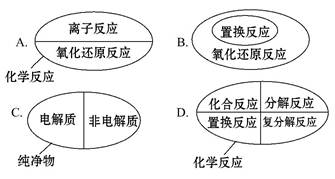
设NA为阿伏加德罗常数的值,下列说法正确的是
| A.在常温常压下,2.8 g N2和CO的混合气体所含电子数为1.4NA |
| B.1 molCl2与足量Fe完全反应,转移3NA个电子 |
| C.1 L 0.1 mol·L-1 NaHCO3溶液中含有0.1 NA个HCO3— |
| D.7.8g Na2O2中阴离子数为0.2NA |