某混合碱是①Na2CO3和NaHCO3或② Na2CO3和 NaOH。用“双指示剂法”对样品的组分和总碱量 [n (Na2O) ] 进行测定。实验方案:称取 0.2960g 样品配成 500mL 溶液,取25.00mL置于250mL 锥形瓶中,加适量蒸馆水和几滴酚酞,用0.0100 mol•L-1的盐酸标准溶液将混合碱滴定成NaHCO3,然后再用溴甲酚绿——二甲基黄为指示剂进行滴定,将NaHCO3完全中和。
(1)某同学平行滴定了三次,每次滴定从 "0" 点开始读数,其中第 I 次滴定的第一个终点的液面如右图所示,请读出实验数据,填入下列表格中
| 序号 |
第一滴定终点的读数(V1/mL) |
第二滴定终点的读数(V2/mL) |
| I |
? |
26.85 |
| II |
10.02 |
25.02 |
| III |
9.98 |
24.98 |
(2)该混合碱样品的组成为 ,理由 。
(3)将混合碱滴定成NaHCO3的过程中,为了结果更加准确,应始终逐滴滴加,这样操作的原因是 。
(4)上述碱样中总碱量[n (Na2O) ]是多少?写出计算过程
。
(5)如果本实验只测定样品的总碱量,实验方案应该怎样设计:
。
A、B、C为短周期元素,在周期表中所处位置如右图所示,A、C两种元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等。
(1)写出A、B、C三种元素的名称:_____、_____、_____。
(2)B位于元素周期表中第_____周期,第_____族。
(3)C的原子结构示意图为_____,C的单质与水反应的化学方程式为_______________。
(4)比较B、C的原子半径_____,写出A的气态氢化物与B的最高价氧化物对应水化物反应的化学方程式____________________。
某元素R有4个电子层,最外层上有5个电子,指出:
(1)R在第_____周期,第_____族,元素符号_____。
(2)R的最高正价_____,负价_____,最高价氧化物化学式_____,对应水化物化学式_____,氢化物化学式_____。
实验室为验证同主族元素性质递变规律,准备了如下药品:
①AgNO3(aq)②稀HNO3③Br2(aq)④I2(aq)⑤NaOH(aq)⑥NaCl(aq)⑦NaBr(aq)⑧H2O⑨Na⑩镁条⑪铝条⑫K
(1)你准备选用的药品是(用编号表示)______。
(2)你所做的实验是什么(用方程式表示)?判断依据是什么?
X、Y、Q、R是同一短周期的元素。已知:
(1)X的最高正价绝对值是最低负价绝对值的3倍,其气态氢化物与最高价氧化物的相对分子质量之比是1∶2.35。
(2)Y和Q的气态氢化物分子组成分别是YH4和QH3。R的氢化物化学式为RH2,但常温时不是气态的。
(3)另有一种元素E,其阳离子和X的阴离子带有等量的相反电荷,且核外电子数相同。请指出X、Y、Q、R、E各是什么元素以及它们在元素周期表中的位置。
将某文献资料上记载的相对原子质量数据摘录如下: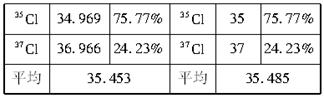
试完成下列问题:
(1)34.969是表示_____________________。
(2)35.453是表示_____________________。
(3)35是表示_________________________。
(4)35.485是表示_____________________。