下列溶液中各微粒的浓度关系或说法正确的是 A.0.1 mol•L-1 pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-)
A.0.1 mol•L-1 pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-) B.等物质的量浓度的下列溶液中,①NH4Al(SO4)2、②NH4Cl、③CH3COONH4、④NH3·H2O;c(NH4+) 由大到小的顺序是:①>②>③>④
B.等物质的量浓度的下列溶液中,①NH4Al(SO4)2、②NH4Cl、③CH3COONH4、④NH3·H2O;c(NH4+) 由大到小的顺序是:①>②>③>④ C.amol·L-1HCN溶液与bmol·L-1NaOH溶液等体积混合后,所得溶液中c(Na+)>c(CN-),则a一定大于b
C.amol·L-1HCN溶液与bmol·L-1NaOH溶液等体积混合后,所得溶液中c(Na+)>c(CN-),则a一定大于b D.0.1mol·L-1的醋酸的pH=a,0.01mol·L-1的醋酸的pH=b,则a+1=b
D.0.1mol·L-1的醋酸的pH=a,0.01mol·L-1的醋酸的pH=b,则a+1=b
下列根据操作和现象或目的所得出的结论正确的是
| 选项 |
操作 |
现象或目的 |
结论 |
| A |
工业上,将BaSO4浸泡在饱和Na2CO3溶液中 |
将BaSO4转化为BaCO3 |
Ksp(BaSO4)>Ksp(BaCO3) |
| B |
向NaAlO2溶液中滴入NaHCO3 |
有白色沉淀 |
AlO结合H+能力比CO强 |
| C |
向PbO2中滴入浓盐酸 |
有黄绿色气体 |
PbO2具有还原性 |
| D |
向鸡蛋白溶液中滴入HgCl2溶液 |
有白色沉淀 |
蛋白质发生盐析 |
菠萝酯常用作化妆品香料,其合成方法如下: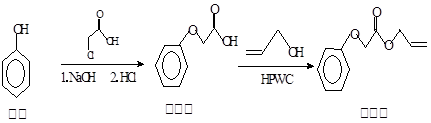
下列说法正确的是
| A.原料苯酚能和NaHCO3溶液反应 |
| B.菠萝酯可以使溴水、高锰酸钾溶液褪色 |
| C.中间体中所有的原子都可以共平面 |
| D.中间体和菠萝酯中均不含手性碳原子 |
下列有关说法正确的是
| A.一定条件下,使用催化剂能加快反应速率但不能改变平衡转化率 |
| B.氢氧燃料电池的能量转换形式仅为化学能转化为电能 |
| C.在NH4HSO4溶液中由于NH4+的水解促进了水的电离,所以水的电离程度增大 |
D.在一密闭容器中发生2SO2+O2 2SO3反应,增大压强,平衡会正向移动, 2SO3反应,增大压强,平衡会正向移动,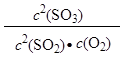 的值增大 的值增大 |
下列表示对应化学反应的离子方程式不正确的是
| A.FeCl3溶液与Cu的反应:Cu+2Fe3+=Cu2++2Fe2+ |
B.向NaClO溶液中加入浓盐酸:ClO +Cl +Cl +2H+=Cl2↑+ H2O +2H+=Cl2↑+ H2O |
C.用氨水溶解Cu(OH)2:Cu(OH)2+4NH3·H2O=[Cu(NH3)4]2++2OH +4H2O +4H2O |
D.向NH4HCO3中滴加少量的NaOH溶液:NH +OH +OH =NH3·H2O+H2O =NH3·H2O+H2O |
下表各组物质之间通过一步反应不可以实现如下图所示转化关系的是
选项 |
X |
Y |
Z |
箭头上所标 数字的反应条件 |
| A |
SiO2 |
Na2SiO3 |
H2SiO3 |
①与Na2CO3熔融 |
| B |
NaCl |
NaHCO3 |
Na2CO3 |
②加热 |
| C |
N2 |
NO2 |
HNO3 |
③加热 |
| D |
C |
CO |
CO2 |
④灼热炭粉 |