:如图所示,在一定温度下,把2体积N2和6体积H2通入一个带有活塞的容积可变的容器中,活塞的一端与大气相通,容器中发生以下反应: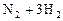

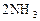 (正反应放热),若反应达到平衡后,测得混合气体的体积为7体积。据此回答下列问题:
(正反应放热),若反应达到平衡后,测得混合气体的体积为7体积。据此回答下列问题: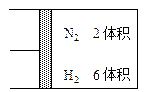
(1)保持上述反应温度不变,设a、b、c分别代表初始加入的N2、H2和NH3的体积,如果反应达到平衡后混合气体中各气体的体积分数仍与上述平衡相同,那么:
①若a=1,c=2,则b=_________。在此情况下,反应起始时将向_________(填“正”或“逆”)反应方向进行。
②若需规定起始时反应向逆反应方向进行,则c的取值范围是_________。
(2)在上述装置中,若需控制平衡后混合气体为6.5体积,则可采取的措施是_________,原因是_________。
某河道两旁有甲、乙两厂。它们排放的工业废水中,共含K+、Ag+、Fe3+、Cl-、OH-、NO3-六种离子。
(1)甲厂的废水明显呈碱性,故甲厂废水所含的三种离子是______、_______、_______。
(2)乙厂的废水中含有另外三种离子。如果加一定量________(选填:活性炭、硫酸亚铁、硫酸亚铁、铁粉),可能回收其中的金属__________(填元素符号)
(3)另一种设想是将甲厂和乙厂的废水按适当的比例混合,可以使废水中的__________(填入离子符号)转化为沉淀。经过滤后的废水主要含_____________,可用来浇灌农田。
淀粉的化学式是:;油脂在体内水解后的产物是:
体内缺乏易造成甲状腺肿大的元素是易患龋齿的元素的是。
氯系消毒剂的作用原理:__________________________
明矾净水原理(方程式)_____________________________
漂白粉失效原理(方程式): ___________________________
硬 水软化的方法有:,。写出煮沸法减小硬度的方程式:, ,
水软化的方法有:,。写出煮沸法减小硬度的方程式:, ,
常见的染发剂可分为、、等三大类。