钢铁工业对促进经济和社会发展起了重要作用。



 (1)炼铁高炉分为五部分,铁矿石与高温煤气主要在部分发生反应,在部分开始生成铁和炉渣。
(1)炼铁高炉分为五部分,铁矿石与高温煤气主要在部分发生反应,在部分开始生成铁和炉渣。
 (2)炼钢时,除磷的化学方程式为;
(2)炼钢时,除磷的化学方程式为;
 加入硅、锰和铝的目的是。
加入硅、锰和铝的目的是。
 (3)不锈钢含有的Cr元素是在炼钢过程的氧吹(填"前"或"后")加入,原因是。
(3)不锈钢含有的Cr元素是在炼钢过程的氧吹(填"前"或"后")加入,原因是。
 (4)炼铁和炼钢生产中,尾气均含有的主要污染物是。
(4)炼铁和炼钢生产中,尾气均含有的主要污染物是。
 从环保和经济角度考虑,上述尾气经处理可用作。
从环保和经济角度考虑,上述尾气经处理可用作。
下列四种装置中,均盛200mL的溶液。
①0.005 mol/LCuSO4溶液,②0.01 mol/LH2SO4,③ZnCl2溶液,④KCl溶液.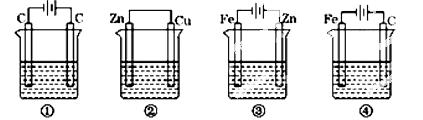
(1)上述四种装置中,为电解池的是(用编号回答),装置①中两电极的电极反应式分别是:阴极:,阳极:;
(2)若将装置④中的外加电源拆去,用导线将两个电极连接,则Fe极上发生的反应是___________________,C极上发生的反应是 。
(3)工作一段时间后,测得导线上均通过0.002mol电子,则上述装置②中生成气体的体积是________ mL (标准状况);
(1)已知:H2(g)+O2(g) H2O(g),反应过程中能量变化如图所示,则:
H2O(g),反应过程中能量变化如图所示,则: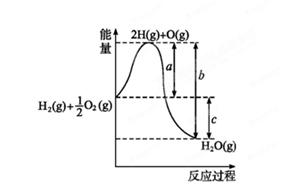
①试写出a、b、c分别代表的意义:
a ;
b ;
c 。
②该反应是反应(填“吸热”或“放热”),ΔH 0(填“>”或“<”)。
(2)发射“天宫”一号的火箭使用的推进剂是液氢和液氧,这种推进剂的优点是 , 。(请写两条)
(3)已知:H2(g)+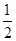 O2(g)=H2O(l) ΔH="-285.8" kJ·mol-1
O2(g)=H2O(l) ΔH="-285.8" kJ·mol-1
H2(g)==H2(l) ΔH="-0.92" kJ·mol-1
O2(g)==O2(l) ΔH="-6.84" kJ·mol-1
H2O(l)=H2O(g) ΔH="+44.0" kJ·mol-1
请写出液氢和液氧生成气态水的热化学方程式:。
写出下列反应的离子方程式
(1)含少量NaHCO3的溶液与含过量Ba(OH)2的溶液混合: ;
(2)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式 ;
(3)硫酸铜溶液和氢氧化钡溶液混合
(4)用醋酸除去水壶中的水垢
(1)通常用小苏打的悬浊液除去CO2中的HCl,反应的离子方程式为:,
不能用NaOH溶液的原因是,也不能用Na2CO3的原因是(均用离子方程式表示原因)
(2).把下列离子方程式改写成化学方程式:
CO32- + 2H+ = CO2↑ + H2O
Ag+ + Cl-= AgCl↓
(1)下列各组中的两种有机物,可能是相同的物质、同系物或同分异构体等,请判断它们之间的关系
①2-甲基丁烷和丁烷。
②1-已烯和环已烷。
(2)支链只有一个乙基且式量最小的烷烃的结构简式。
(3)写出乙醛溶液与足量的银氨溶液共热的化学方程式:;
(4)写出1,3-丁二烯与溴单质发生1,4-加成的反应方程式
(5)写出由乙醇一步制溴乙烷的化学方程式