下列说法都正确的是
①江河入海口三角洲的形成通常与胶体的性质有关
②四川灾区重建使用了大量钢材,钢材是合金
③“钡餐”中使用的硫酸钡是弱点解质
④太阳能电池板中的硅在元素周期表中处于金属与非金属的交界位置
⑤常用的自来水消毒剂有氯气和二氧化氮,两者都含有极性键
⑥水陆两用公共汽车中,用于密封的橡胶材料是高分子化合物
| A.①②③④ | B.①②④⑥ | C.①②⑤⑥ | D.③④⑤⑥ |
铅蓄电池的电池反应为 Pb(s)+PbO2(s)+2H2SO4(aq)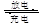 2PbSO4(s)+2H2O(l),下列说法错误的是
2PbSO4(s)+2H2O(l),下列说法错误的是
| A.放电时覆盖PbO2的电极为正极,发生还原反应 |
| B.放电时电解质溶液中的H+向正极移动 |
| C.充电时阴极的电极反应为 PbSO4(s) + 2e-="Pb(s)" + SO42-(aq) |
| D.充电时电解质溶液的pH逐渐增大 |
已知反应 ①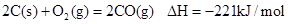
②稀溶液中,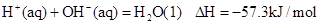 ,下列结论正确的是
,下列结论正确的是
| A.碳的燃烧热△H为110.5kJ/mol |
| B.2molC(s)和1molO2(g)的能量比2molCO(g)的能量高221kJ |
| C.0.5 molH2SO4(浓)与1 molNaOH溶液混合,产生57.3kJ热量 |
| D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3kJ热量 |
下列说法中,正确的是
| A.某离子被沉淀完全是指该离子在溶液中的浓度变为0 |
| B.某物质的溶解性为难溶,则该物质的溶解度为0 |
| C.一般来说,溶解度小的难溶物容易转化为溶解度大的难溶物 |
| D.沉淀的生成、溶解和转化其实质都是沉淀发生了溶解平衡的移动 |
已知在某密闭容器中发生反应 4NH3+5O2=4NO+6H2O,若反应速率分别用υ(NH3)、υ(O2)、υ(NO)、υ(H2O)表示,则下列关系正确的是
A.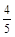 υ(NH3) =υ(O2) υ(NH3) =υ(O2) |
B.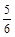 υ(O2) =υ(H2O) υ(O2) =υ(H2O) |
C.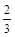 υ(NH3) =υ(H2O) υ(NH3) =υ(H2O) |
D.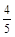 υ(O2) =υ(NO) υ(O2) =υ(NO) |
下列关于原电池、电解池的叙述中正确的是
| A.发生氧化反应的电极分别为负极和阴极 |
| B.阴离子分别向负极和阴极迁移 |
| C.电子流向分别由负极直接流向正极、阴极直接流向阳极 |
| D.若都有一个电极质量减轻,应分别为负极和阳极 |