下列叙述正确的是(用NA代表阿伏加德罗常数的值)

A.2.4g金属镁变为镁离子时失去的电子数为0.1NA  |
B.1molHCl气体中的粒子数与0.5 mo1/L盐酸中溶质粒子数相等  |
C.在标准状况下,22.4LCH4与18gH2O所含有的电子数均为10 NA  |
D.CO和N2为等电子体,22.4L的CO气体与lmol N2所含的电子数相等 |
常温下,有下列四种溶液:
| ① |
② |
③ |
④ |
| 0.1mol/L NaOH溶液 |
pH = 11 NaOH溶液 |
0.1mol/L CH3COOH溶液 |
pH = 3 CH3COOH溶液 |
下列说法正确的是( )
A.由水电离出的c(H+):①>③
B.③稀释到原来的100倍后,pH与④相同
C.①与③混合,若溶液pH = 7,则V(NaOH)>V(CH3COOH)
D.②与④混合,若溶液显酸性,则所得溶液中离子浓度可能为: c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
电解100mL含 c(H+)=0.30mol/L的下列溶液,当电路中通过0.04mol电子时,理论上析出金属质量最大的是()
| A.0.10mol/LAg+ | B.0.20mol/L Zn2+ | C.0.20mol/L Cu2+ | D.0.20mol/L Pb2+ |
将1molCO和1molNO2充入密闭容器中,在催化剂存在下发生反应 NO2(g)+CO(g) CO2(g)+NO(g)并达到化学平衡,发现有50%的CO转化为CO2。在其它条件不变的情况下,若将1molCO和2molNO2充入上述反应器中,则反应达到化学平衡时,混合气体中CO2的体积分数是()
CO2(g)+NO(g)并达到化学平衡,发现有50%的CO转化为CO2。在其它条件不变的情况下,若将1molCO和2molNO2充入上述反应器中,则反应达到化学平衡时,混合气体中CO2的体积分数是()
A.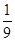 |
B.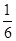 |
C.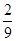 |
D.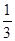 |
在某容积一定的密闭容器中,可逆反应:A(g)+B(g) xC(g),符合下列图象(Ⅰ)所示关系.由此推断对图(Ⅱ)的正确说法是()
xC(g),符合下列图象(Ⅰ)所示关系.由此推断对图(Ⅱ)的正确说法是()
| A.p3>p4,Y轴表示A的质量 | B.p3>p4,Y轴表示混合气体平均摩尔质量 |
| C.p3>p4,Y轴表示混合气体密度 | D.p3<p4,Y轴表示B的百分含量 |
已知某温度下,Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=1×10-12,下列叙述正确的是()
| A.饱和AgCl溶液与饱和Ag2CrO4溶液相比,前者的c(Ag+)大 |
| B.向氯化银的浊液中加入氯化钠溶液,氯化银的Ksp减小 |
| C.向0.0008 mol·L- 1的K2CrO4溶液中加入等体积的0.002mol/LAgNO3 溶液,则CrO42-完全沉淀 |
| D.将0.001 mol·L- 1的AgNO3 溶液滴入0.001 mol·L- 1的KCl和0.001 mol·L- 1的K2CrO4溶液,则先产生AgCl沉淀 |