C、S、O、Se是同族元素,该族元素单质及其化合物在材料、医药等方面有重要应用。请回答下列问题:
(1)Ge的原子核外电子排布式为








(2)C、Si、Sa三种元素的单质中,能够形成金属晶体的是
(3)按要求指出下列氧化物的空间构型、成键方式或性质
①CO2分子的空间构型及碳氧之间的成键方式 ;
②SO2晶体的空间构型及硅氧之间的成键方式 ;
 ③已知SnO2是离子晶体,写出其主要物理性质 (写出2条即可)
③已知SnO2是离子晶体,写出其主要物理性质 (写出2条即可)
(4)CO可以和很多金属形成配合物,如Ni(CO)2,Ni与CO之间的键型为
(5)碳氧键的红外伸缩振动频率与键的强度成正比,已知Ni(CO)4中碳氧键的伸缩振动频率为2060cm-3,CO分子中碳氧键的伸缩振动频率为2143cm-2,则Ni(CO)中碳氧键的强度比CO分子中碳氧键的强度 (填字母)
A.强
B.弱
C.相等
D.无法判断
食盐是日常生活的必需品,也是重要的化工原料。
(1)粗食盐常含有少量Ca2 +、Mg2+、SO42-等杂质离子,实验室提纯NaCl的流程如下:
+、Mg2+、SO42-等杂质离子,实验室提纯NaCl的流程如下: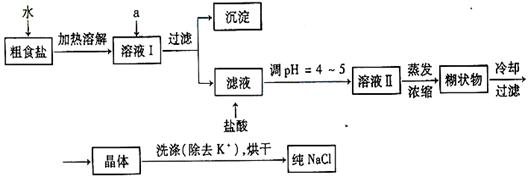 提供的试剂如下:饱和Na2CO3溶液饱和K2CO3溶液 NaOH溶液 BaCl2溶液 Ba(NO3)2溶液
提供的试剂如下:饱和Na2CO3溶液饱和K2CO3溶液 NaOH溶液 BaCl2溶液 Ba(NO3)2溶液
欲除去溶液Ⅰ中的Ca2+、Mg2+、SO42-离子,选出a所代表的多种试剂,按滴加顺序依次为。(只填化学式)
(2)电解饱和食盐水的装置如图所示,如果在饱和食盐水中滴加酚酞,通电后(填X或Y)极附近溶液变红,写出电解饱和食盐水的化学方程式。
(3)实验室制备H2和Cl2通常采用下列反应:
Zn+H2SO4====ZnSO4+H2↑
MnO2+4H Cl(浓)
Cl(浓)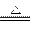 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
据此,从下列所给仪器装置中选择制备并收集H2的装置 (填代号)和制备并收集干燥、纯净Cl2的装置
(填代号)和制备并收集干燥、纯净Cl2的装置 (填代号)。
(填代号)。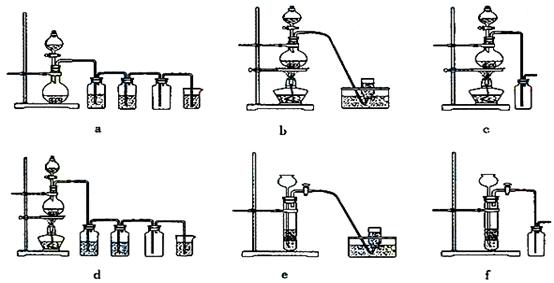
某澄清溶液,可能含有NH4+ 、Na+、K+、Cl-、CO32-、SO42-中的一种或几种,现做如下实验:
、Na+、K+、Cl-、CO32-、SO42-中的一种或几种,现做如下实验:
①取少量该溶液加入BaC l2溶液有白色沉淀生成,再加入足量盐酸后,沉淀部分溶解,并有气体生成。
l2溶液有白色沉淀生成,再加入足量盐酸后,沉淀部分溶解,并有气体生成。
②用铂丝蘸取少量该溶液置于无色酒精灯火焰中灼烧,火焰呈黄色,透过蓝色钴玻璃观察,未见紫色火焰。
③另取少量该溶液加入NaOH溶液并加热,将湿润的红色石蕊试纸靠近试管口无颜色变化。
(1)第①步可以检验出的离子是
(2)第②③步说明一定含有的离子是
(3)从以上操作中,不能判断是否存在的离子是 ,为了检验该离子是否存在,请你写出进一步检验的 操作步骤和实验现象:
操作步骤和实验现象:
有A、B、C、D、E五种元素,它们原子的核电荷数依次递增且均小于18;
A原子核内仅有1个质子;B原子的电子总数与C原子的最外层电子数相等; C原子有两个电子层,最外层电子数是次外层电子数的3倍;D元素的最外层电子数是其电子层数的三分之一。E的单质是黄绿色气体且有毒。
(1)写出A分别与B、C所形成化合物的化学式:,。
(2)分别写出C和D的原子结构示意图:,。
(3)写出C、D、E所形成的化合物的电离方程式:。
(4)写出E的单质与A、C、D三元素所形成的化合物反应的化学方程式,若是氧化还原反应,请用双线桥标出电子转移的数目和方向:。
同温同压下,若A容器中充满O2 ,B容器中充满O3。
(1)若所含分子总数相等,则A容器和B容器的容积之比是
(2)若两容器中所含原子总数相等,则A容器和B容器的容积比是
(3)若两容器的体积比为3∶2,则O2和O3物质的量之比为_________,质量之比为_______,密度之比为______________。
(3分)A元素的原子最外层有3个电子,B元素的原子最外层有7个电子,当它们失去或得到电子形成稳定结构时,A的化合价为________,B的化合价为____ _____,A与B结合形成化合物的化学式为_______________。
_____,A与B结合形成化合物的化学式为_______________。