下列实验操作中,正确的是
①用托盘天平称取5.2 g NaCl;②用50 mL量筒量取5.2mL盐酸;③用蒸发皿加热NaCl溶液可以得到Nacl晶体;④用 100 mL容量瓶配制50 mL 0.1mol·L-1H2SO4溶液;⑤用带玻璃塞的棕色试剂瓶存放浓HNO3;⑥中和热测定的实验中使用的玻璃仪器只有2种
| A.①③⑤ | B.②④⑥ | C.①③④ | D.③⑤⑥ |
分别放置在如图所示装置(都盛有0.1 mol·L-1的H2SO4溶液)中的四个相同的纯锌片,腐蚀最慢的是 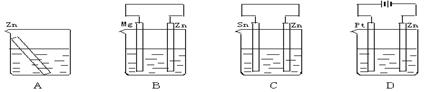
已知450℃时,反应H2(g)+I2(g)  2HI(g)的K=50,由此推测在450℃时,反应2HI(g)
2HI(g)的K=50,由此推测在450℃时,反应2HI(g)  H2(g)+I2(g)的化学平衡常 数为
H2(g)+I2(g)的化学平衡常 数为
| A.0.02 | B.50 | C.100 | D.无法确定 |
一定条件下,在2 L的密闭容器中通入4.0 mol的N2和适量的H2,发生反应:N2(g)+3H2(g) 2NH3(g)。经过5s后,测得N2剩余2.0 mol,在这5S内N2的反应速率为
2NH3(g)。经过5s后,测得N2剩余2.0 mol,在这5S内N2的反应速率为
A.0.3 mol L-1 L-1 s-1 s-1 |
B.0.2mol L-1 L-1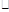 s-1 s-1 |
C.0.4 mol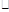 L-1 L-1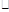 s-1 s-1 |
D.0.5 mol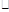 L-1 L-1 s-1 s-1 |
下列各组离子在溶液中能大量共存的是
| A.Fe2+、NH4+、SO42—、S2— | B.Al3+、AlO2—、HCO3—、Na+ |
| C.Ca2+、HCO3—、Cl—、K+ | D. Fe3+、SCN—、Na+、CO32— |
强酸与强碱的稀溶液发生中和反应时,中和热的热化学方程式可表示为:
H+(aq)+OH-(aq)══ H2O(l) ΔH="-57.3" kJ·mol-1。有以下4个化学方程式:
①H2SO4(aq)+2NaOH(aq)══ Na2SO4(aq)+2H2O(l)
②H2SO4(aq)+Ba(OH)2(aq)══ BaSO4(s)+2H2O(l)
③1/2H2SO4(aq)+NaOH(aq)══ 1/2 Na2SO4(aq)+H2O(l)
④1/2H2SO4(浓,aq)+NaOH(aq) ══ 1/2Na2SO4(aq)+H2O(l)
其中反应热为-57.3 kJ·mol-1的是
| A.①② | B.③ | C.④ | D.均不符合 |