1) ;消耗了氯水中的HCl,使
;消耗了氯水中的HCl,使 平衡向右移动,
平衡向右移动, 浓度增大
浓度增大
(2)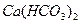 (写名称正确同样得分)
(写名称正确同样得分)
(3)在导管末端再连接长导管,使导管的出口接近量筒底部
(4)碳酸钙与氯水反应生成的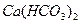 再受热时.除生成
再受热时.除生成 外,还生成了
外,还生成了
(5)从圆底烧瓶蒸出的水蒸气在广口瓶中冷凝、聚集
下列离子方程式书写正确的是
| A.实验室用大理石和稀盐酸制取CO2:2H+ + CO32- = CO2↑+ H2O |
| B.氢氧化钡溶液与浓盐酸反应:OH-+H+= H2O |
| C.三氯化铁溶液中加入铁粉: Fe3++ Fe= 2Fe2+ |
| D.钠投入水中:Na +H2O = Na+ + OH- + H2↑ |
根据下列反应判断氧化剂的氧化性由强到弱的顺序,正确的是
① Cl2+2KI ══ I2+2KCl② 2FeCl3+2HI ══ I2+2FeCl2+2HCl
③ 2FeCl2+Cl2══ 2FeCl3④ I2+SO2+2H2O ══ 2HI+H2SO4
| A.Cl2>I2>Fe3+>SO2 | B.Cl2>Fe3+>I2>SO2 |
| C.Fe3+>Cl2>I2>SO2 | D.Cl2>Fe3+>SO2>I2 |
下列各组中的离子,能在溶液中大量共存的是
| A.H+Na+CO32- Cl- | B.Ba2+ Na+Cl- SO42- |
| C.Ag+ Al3+ NO3-H+ | D.K+ H+ SO42-OH- |
2008年北京奥运会的国家游泳中心(水立方)采用了高分子膜材料“ETFE”,该材料是四氟乙烯(CF2=CF2)与乙烯(CH2=CH2)发生聚合反应得到的高分子材料。下列说法不正确的是
A.“ETFE”分子中可能存在“—CF2—CH2—CF2—CH2—”的连接方 法 法 |
| B.合成“ETFE”的反应为加聚反应 |
| C.CF2=CF2和CH2=CH2均是平面型分子 |
| D.该材料是一种合成高分子材料,不可以与氢气发生加成反应 |
要证明一氯甲烷中氯元素的存在可以进行如下操作,其中顺序正确的是
①加入AgNO3溶液②加入NaOH溶液③加热④加蒸馏水⑤冷却后加入HNO3后酸化⑥加入NaOH的乙醇溶液
| A.④③①⑤ | B.②③⑤① | C.④③① | D.⑥③⑤① |