以铁为阳极、铜为阴极,对足量的NaOH溶液电解,一段时间后,得到2 mol Fe(OH)3沉淀,此间共消耗水的物质的量为( )
| A.3mol | B.4mol | C.5mol | D.6mol |
氢氰酸(HCN)的下列性质中,不能证明它是弱电解质的是
| A.1 mol/L氢氰酸溶液的pH约为3 |
| B.常温下,pH=a的HCN稀释100倍后所得溶液pH<(a +2)[(a +2)<7] |
| C.10 mL 1 mol/L HCN恰好与10 mL 1 mol/L NaOH溶液完全反应 |
| D.NaCN溶液呈碱性 |
甲醇(CH3OH)燃料电池可用作电动汽车电源,下图为电池示意图。在电池的一极通入甲醇,另一极通入氧气,工作时H+由负极移向正极。下列叙述不正确的是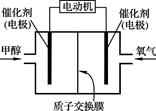
| A.外电路通过0.6 mol电子时,理论上消耗甲醇3.2 g |
| B.通甲醇一端为负极 |
| C.正极反应为:O2+4H++4e-= 2H2O |
| D.负极反应为:CH3OH+H2O+6e-= CO2↑+6H+ |
下列有关问题,与盐的水解有关的是
① NH4Cl与ZnCl2溶液可作焊接金属中的除锈剂
② 用NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂
③ 草木灰与铵态氮肥不能混合施用
④ 实验室盛放碳酸钠溶液的试剂瓶不能用磨口玻璃塞
⑤ 加热蒸干AlCl3溶液得到Al(OH)3固体
| A.①②③ | B.②③④ | C.①④⑤ | D.①②③④⑤ |
常温下,pH都等于9的NaOH溶液和CH3COONa两种溶液中,若由水电离产生OH-浓度分别为a mol/L和b mol/L,则a和b的关系是
| A.a>b | B.a=10-4b | C.b=10-4a | D.a=b |
物质的量浓度相同的三种盐NaX、NaY和NaZ的溶液,其pH值依次为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序是
| A.HX、HY、HZ | B.HZ、HY、HX |
| C.HX、HZ、HY | D.HY、HZ、HX |