如右图所示装置,两玻璃管中盛满滴有酚酞溶液的NaCl饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极。接通S1后,C(Ⅰ)附近溶液变红,两玻璃管中有气体生成。一段时间后(两玻璃管中液面未脱离电极),断开S1,接通S2,电流表的指针发生偏转,说明此时该装置形成了原电池,关于该原电池的叙述正确的是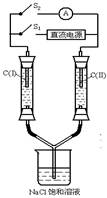
| A.C(I)的电极反应式是2H++2e- = H2↑ |
| B.C(II)的电极反应式是Cl2+2e-=2Cl- |
| C.C(I)的电极名称是阴极 |
| D.C(II)的电极名称是负极 |
下列有关晶体的说法中正确的是
| A.某晶体固态不导电,水溶液能导电说明该晶体是离子晶体 |
| B.原子晶体的原子间只存在共价键,而分子晶体内只存在范德华力。 |
| C.区分晶体和非晶体最科学的方法是对固体进行X-射线衍射实验 |
| D.任何晶体中,若含有阳离子也一定含有阴离子 |
石墨晶体是层状结构,在每一层内;每一个碳原于都跟其他3个碳原子相结合,如图是其晶体结构的俯视图,则图中7个六元环完全占有的碳原子数是 
| A.10个 | B.14个 | C.18个 | D.21个 |
下列对分子性质的解释中,不正确的是
| A.碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释 |
B.由于乳酸(  )中存在一个手性碳原子,导致该物质存在互为镜像的两个 )中存在一个手性碳原子,导致该物质存在互为镜像的两个手性异构体;生产中可利用“手性合成”法主要得到其中一种手性分子 |
| C.HF的稳定性很强,是因为其分子间能形成氢键 |
| D.由下图可知酸性:H3PO4>HClO,因为H3PO4分子中有1个非羟基氧原子 |

0.01mol氯化铬(CrCl3·6H2O)在水溶液中用过量的AgNO3溶液处理,产生0.02molAgCl沉淀,此氯化铬最可能为
| A.[Cr(H2O)6] Cl3 | B.[Cr(H2O)3Cl3]·3H2O |
| C.[Cr(H2O)4Cl2] Cl·2H2O | D.[Cr(H2O)5 Cl] Cl2·H2O |
向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液。下列对此现象说法正确的是
| A.反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 |
| B.沉淀溶解后,生成深蓝色溶液是由于存在配合离子[Cu(NH3)4]2+ |
| C.向反应后的溶液中加入乙醇,将析出深蓝色的晶体CuSO4·5H2O |
| D.在[Cu(NH3)4]2+离子中,既存在离子键,又存在共价键 |