高温下硫酸亚铁发生如下反应:
2FeSO4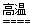 Fe2O3+SO2↑+SO3↑,若将生成的气体通入氯化钡溶液中,得到的沉淀物是
Fe2O3+SO2↑+SO3↑,若将生成的气体通入氯化钡溶液中,得到的沉淀物是
| A.BaSO3和BaSO4 | B.BaS |
| C.BaSO3 | D.BaSO4 |
“绿色化学实验”已走进课堂,下列做法符合“绿色化学”的是()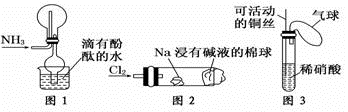
①实验室收集氨气采用图1所示装置
②实验室中做氯气与钠反应实验时采用图2所示装置
③实验室中采用图3所示装置进行铜与稀硝酸的反应
④实验室中用玻璃棒分别蘸取浓盐酸和浓氨水做氨气与酸生成铵盐的实验
| A.②③④ | B.①②④ | C.①②③ | D.①③④ |
已知:SO2(g)+1/2O2(g) 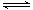 SO3, ΔH = -98kJ/mol。某温度下,向一体积为2L的密闭容器中充入0.2mol SO2和0.1mol O2,5min后达到平衡,共放出热量11.76kJ,下列说法正确的是()
SO3, ΔH = -98kJ/mol。某温度下,向一体积为2L的密闭容器中充入0.2mol SO2和0.1mol O2,5min后达到平衡,共放出热量11.76kJ,下列说法正确的是()
| A.5min内用O2表示的反应速率为0.12mol/(L·min) |
| B.该反应的平衡常数数值为7.5 |
| C.SO2的平衡转化率为60% |
| D.加入催化剂,可使ΔH变小 |
甲~庚等元素在周期表中的相对位置如下表,己的最高氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数。下列判断正确的是()
| A.丙与戊的原子序数相差28 |
| B.气态氢化物的稳定性:庚<己<戊 |
| C.常温下,甲和乙的单质均能与水剧烈反应 |
| D.丁的最高价氧化物不与任何酸反应 |
25℃、101kPa下,碳、氢气和甲烷的燃烧热依次是393.5 kJ·mol—1、285.8 kJ·mol—1
和890.3kJ·mol—1,下列选项中正确的是()
| A.2H2(g)+O2(g)=2H2O(l)△H=—285.8kJ·mol—1 |
| B.CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=+890.3kJ·mol—1 |
| C.H2(g)+1/2O2(g)=H2O(g)△H<—285.8kJ·mol—1 |
| D.C(s)+2H2(g)=CH4(g)△H=—74.8 kJ·mol—1 |
化学与生产、生活息息相关,下列叙述错误的是()
| A.碱性锌锰干电池比普通锌锰干电池性能好,比能量和可储存时间均有提高 |
| B.汽车加大油门、把食物放在冰箱里,食品包装袋内放置小包除氧剂,都是为了改变反应物转化率而采取的措施 |
| C.1kg人体脂肪可存储约32200kJ能量,一般人每行走1km大约要消耗170kJ能量,如果每天步行5km,一年(按365天计)中消耗的脂肪大约是9.6kg |
| D.炒菜用铁锅未及时洗净(残余中含NaCl),可能发生电化学腐蚀生成红褪色锈斑 |