设NA表示阿伏加德罗常数的值,下列有关NA的叙述中正确的有
①标准状况下,20 g重水(D2O)中含有的电子数为10NA
②0.5 mol Fe2+与足量的H2O2溶液反应,转移0.5 NA个电子
③将2 mol NO和1 mol O2混合后,体系中的分子总数为3NA
④乙烯和环丙烷组成的42 g混合气体中氢原子的个数为6NA
⑤2 mol·L-1碳酸钠溶液中Na+的数目是2NA
⑥1 mol氯气溶解在水中得到的新制氯水中氢离子的数目是NA
⑦22.4 L的N2的共用电子对数为3NA
| A.3个 | B.4个 | C.5个 | D.全部正确 |
下列实验能达到目的的是
| A.只滴加氨水鉴别NaCl、AlCl3、MgCl2、Na2SO4四种溶液 |
| B.将NH4Cl溶液蒸干制备NH4Cl固体 |
| C.用萃取分液的方法除去酒精中的水 |
| D.用可见光束照射以区别溶液和胶体 |
为实现下列实验目的,依据下表提供的主要仪器,所用试剂合理的是
| 选项 |
实验目的 |
主要仪器 |
试剂 |
| A |
分离Br2和CCl4的混合物 |
分液漏斗、烧杯 |
Br2和CCl4的混合物、蒸馏水 |
| B |
实验室制取H2 |
试管、带导管的橡皮塞 |
锌粒、稀HNO3 |
| C |
鉴别葡萄糖和蔗糖 |
试管、烧杯、酒精灯 |
葡萄糖溶液、蔗糖溶液、 银氨溶液 |
| D |
测定NaOH溶液的浓度 |
滴定管、锥形瓶、烧杯 |
NaOH溶液、 0.100 0 mol·L-1盐酸 |
下列选用的相关仪器符合实验要求的是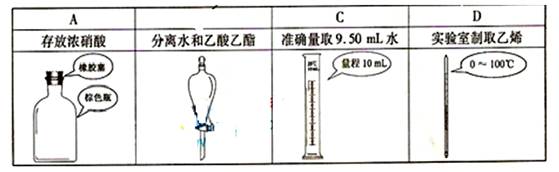
下图是CO2电催化还原为CH4的工作原理示意图。下列说法不正确的是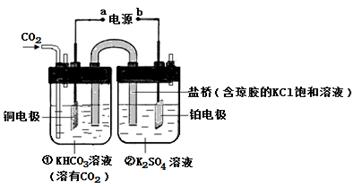
| A.该过程是电能转化为化学能的过程 |
| B.一段时间后,①池中n(KHCO3)不变 |
| C.一段时间后,②池中溶液的pH一定下降 |
| D.铜电极的电极反应式为CO2+8H++8e-=CH4+2H2O |