KClO3与浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯。其变化可表述为:
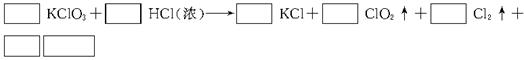
(1)请完成该化学方程式并配平(未知物化学式和系数填入框内)。
(2)浓盐酸在反应中显示出来的性质是 (填写编号,多选倒扣)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)产生0.1 mol Cl2,则转移的电子的物质的量为___________mol。
(4)ClO2具有很强的氧化性。因此,常被用作消毒剂,其消毒的效率(以单位质量得到的电子数表示)是Cl2的 倍。
(福建省漳州市芗城中学2009届高三一轮复习单元测试,化学,25)实验室用密度为1.18g/mL,质量分数为36.5%浓盐酸配制250mL0.1mol/L的盐酸溶液,填空并请回答下列问题:
(1)配制250mL0.1mol/L的盐酸溶液。应量取盐酸体积_______mL,应选用容量瓶的规格_________mL。除容量瓶外还需要的其它仪器_________________________________。
(2)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)____________________
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
B.用量筒量准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入250mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1—2cm处
(3) 操作A中,将洗涤液都移入容量瓶,其目的是
。溶液注入容量瓶前需恢复到室温,这是因为
。
(4)若出现如下情况,对所配溶液浓度将有何影响(偏高、偏低或无影响)?
a.没有进行A操作__________;b.加蒸馏水时不慎超过了刻度________;c.定容时俯视____________。
(5)若实验过程中出现如下情况如何处理?
加蒸馏水时不慎超过了刻度? __________________。
向容量瓶中转移溶液时(实验步骤B) 不慎有液滴掉在容量瓶外? _______ _______。
(安徽省合肥八中2008—2009学年度高三第二次月考,化学,18)用6mol·L-1的硫酸配制100mL1.0mol·L-1硫酸,若实验仪器有:
A.100mL量筒 B.托盘天平 C.玻璃棒 D.50mL容量瓶
E.20mL量筒 F.胶头滴管 G.50mL烧杯 H.100mL容量瓶
(1)实验时应选用仪器的先后顺序是(填入编号)。
(2)在容量瓶的使用方法中,下列操作不正确的是(填写编号)。
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近标线2cm~3cm处,用滴管滴加蒸馏水到标线
D.配制溶液时,如果试样是液体,用量筒取试样后直接倒入容量瓶中,缓慢加入蒸馏水到接近容量瓶刻度标线1cm~2cm处,用滴管滴加蒸馏水到刻度线
E.盖好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转和摇动多次
(3)怎样检查容量瓶是否漏水。
有主族元素A、B、C、D四种元素,原子序数依次递增,A元素原子2p轨道上有2个
未成对电子。B原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元
素所形成的氢化物中最大。C的最高化合价和最低化合价的代数和为4,其最高价氧化物中
含C的质量分数为40%,且其核内质子数等于中子数。D原子得一个电子填入3p轨道后,
3p轨道已充满。








请回答下列问题:
(1)AC2分子中含有____根π键,属于__________分子(填“极性分子”或“非极性分子”)
(2) B的氢化物的空间构型为_________,B原子的原子轨道采用______杂化,其氢化物在同族元素所形成的氢化物中沸点最高的原因是__________。
(3)写出A的常见氧化物与B的氧化物中互为等电子体的一组___________
(4)C元素的电负性_______D元素的电负性(填“>”,“<”或“=”);用一个化学方程式表示__________________________________
已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他4种元素既不在同一周期又不在同一主族。B和C属同一主族,D和E属同一周期,又知E是周期表中1—18列中的第7列元素。D的原子序数比E小5,D跟B可形成离子化合物其晶胞结构如右图。
请回答:
(1)A元素的名称是 ;
(2)B的元素符号是 ,C的元素符号是 ,B与A形成的化合物比C 与A形成的化合物沸点高,其原因是
(3)E属元素周期表中第 周期,第 族的元素,其元素名称是 ,它的+2价离子的电子排布式为 :
(4)从图中可以看出,D跟B形成的离子化合物的化学式为 ;该离子化合物晶体的密度为ag·cm-3,则晶胞的体积是 (只要求列出算式)。
G和Si元素在化学中占有极其重要的地位。
(1)写出Si的基态原子核外电子排布式 。
从电负性角度分析,C、Si和O元素的非金属活泼性由强至弱的顺序为 。
(2)SiC的晶体结构与晶体硅的相似,其中C原子的杂化方式为 ,微粒间存在的作用力是 。
(3)氧化物MO的电子总数与SiC的相等,则M为 (填元素符号),MO是优良的耐高温材料,其晶体结构与NaCl晶体相似,MO的熔点比CaO的高,其原因是 。
(4)C、Si为同一主族的元素,CO2和SiO2化学式相似,但结构和性质有很大不同。CO2中C与O原子间形成σ键和π键,SiO:中Si与O原子间不形成上述π健。从原子半径大小的角度分析,为何C、O原子间能形成,而Si、O原子间不能形成上述π健 。