下列灭火剂能用于扑灭金属钠着火的是
| A.干冰灭火剂 | B.黄砂 |
| C.干粉(含NaHCO3)灭火剂 | D.泡沫灭火剂 |
分子式为C5H8的有机物,其结构不可能是()
| A.只含一个双键的直链有机物 |
| B.含两个双键的直链有机物 |
| C.只含一个双键的环状有机物 |
| D.只含一个三键的直链有机物 |
一种烃的结构可表示为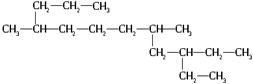
用系统命名法命名,该烃的名称为()
| A.4,8-二甲基-10-乙基12烷 | B.5,9-二甲基-3-乙基十二烷 |
| C.5-甲基-3-乙基-9-丙基十一烷 | D.3,9-二甲基-4-乙基十二烷 |
在烷烃同系物中,含碳元素质量分数最大接近于 ( )
| A.75.0% | B.80.0% | C.85.7% | D.92.3% |
某气态烃0.5mol能与1molHCl完全加成,加成后产物分子上的氢原子又可被3molCl2取代,则此气态烃可能是()
| A.CH≡CH | B.CH≡C-CH3 | C.CH2=CH2 | D.CH2=C(CH3)2 |
设阿伏加德罗常数的值为NA,下列说法中正确的是()
| A.1mol苯乙烯中含有的C=C数为4NA |
| B.2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |
| C.0.1molCnH2n+2中含有的C-C键数为0.1nNA |
| D.标准状况下,2.24LCHCl3含有的分子数为0.1NA |