甲基橙和酚酞在水中和有机溶剂中的溶解度不同,当溶剂沿滤纸流经混合物点样时,甲基橙和酚酞会以不同的速率在滤纸上移动,从而达到分离的目的。某校化学兴趣小组拟通过该原理将甲基橙和酚酞从混合溶液A中分离开来:
步骤Ⅰ 把0.1 g甲基橙和0.1 g酚酞溶解在10mL60%的乙醇溶液里,配制混合溶液A;另将10mL乙醇和4mL浓氨水充分混合,配成混合溶液B;
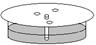
步骤Ⅱ 在一张圆形滤纸中心扎一小孔,将细纸芯插入滤纸中央(如图)。在距滤纸中心约1cm的圆周上,选择三个点,分别用毛细管将A溶液在该三点处点样;
步骤Ⅲ 将滤纸覆盖在盛有B溶液的培养皿上,使滤纸芯与溶液接触,放置一段时间,点样逐渐向外扩散,形成黄环;
步骤Ⅳ 待黄环半径扩散到滤纸半径的二分之一时,取下滤纸,等滤纸稍干后,喷上饱和Na2CO3溶液,通过现象判断分离的效果。
试回答下列问题:
⑴本实验采用的分离方法叫_________,若分离淀粉胶体与氯化钠的混合液则可选用______法;
⑵步骤Ⅱ中若在滤纸上事先作点样位置标记,宜选用_____________笔(填“钢”或“铅”);
⑶步骤Ⅳ中喷洒Na2CO3溶液后,能观察到的现象是__________________________,这说明实验中________在滤纸上移动速率更快(填“甲基橙”或“酚酞”);
⑷他们可以通过_____________________________来判断分离的效果。
A、B、C、D、E五种物质之间的关系如下图所示,其中E为黑色物质,B为气体,C为金属,反应Ⅲ是C在D的稀溶液中进行的,则A为_______,B为______,D为______ 。
写出反应Ⅰ的离子方程式______________________________。
现在工业上主要采用离子交换膜法电解饱和食盐水制取H2、Cl2、NaOH。请完成下列问题:
(1)在电解过程中,与电源正极相连的电极上所发生的电极反应式为________________________________。
(2)电解之前食盐水需要精制,目的是除去粗盐中的Ca2+、Mg2+、SO42+等杂质离子,使用的试剂有:
a.Na2CO3溶液,b.Ba(OH)2溶液,c.稀盐酸,其合理的加入顺序为________________(填试剂序号)。
(3)如果在容积为10 L的离子交换膜电解槽中,1 min在阴极可产生11.2 L(标准状况)Cl2,这时溶液的pH是(设体积维持不变)________。
(4)Cl2常用于自来水的消毒杀菌,现在有一种新型消毒剂ClO2,若它们在杀菌过程中的还原产物均为Cl-,消毒等量的自来水,所需Cl2和ClO2的物质的量之比为________。
如图所示,在大试管里放一段光亮无锈的弯成螺旋状的铁丝,把试管倒插入水中,将这个装置这样放置约一周后,观察到铁丝发生的变化是 _____________________,原因是___________________________________。试管内水面会上升,最终 上升高度大约为_______,原因是__________________________________________________。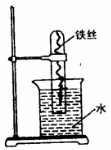
生活中常常有这样的现象:一件普通的铁器,如不精心保管,便会生锈;若不引起注意,锈斑蔓延开来,就会吞噬整个铁器使之变成废物。人们称这种现象为“锈吃铁”。请用相关学科知识解释“锈吃铁”这一自然现象。
请利用氧化还原反应Cu+2FeCl3====2FeCl2+CuCl2设计一个原电池。