| A.同位素 | B.同素异形体 |
| C.同分异构体 | D.同系物 |
对于3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g),反应的化学平衡常数的表达式为( )
Fe3O4(s)+4H2(g),反应的化学平衡常数的表达式为( )
已知(l)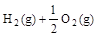 =H2O(g)△H1=a kJ·
=H2O(g)△H1=a kJ·
(2)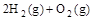 =2H2O(g)△H2=b kJ·
=2H2O(g)△H2=b kJ·
(3)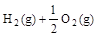 =H2O(l)△H3=c kJ·
=H2O(l)△H3=c kJ·
(4) =2H2O(l)△H4=d kJ·
=2H2O(l)△H4=d kJ·
下列关系式中正确的是()
| A.a<c<0 | B.b>d>0 | C.2a=b<0 | D.2c=d>0 |
实验室进行中和热测定的实验时除需要大烧杯(500 mL)、小烧杯(100 mL)外,所用的其他仪器和试剂均正确的一组是( )
| A.0.50 mol·L-1盐酸,0.50 mol·L-1NaOH溶液,100 mL量筒1个 |
| B.0.50 mol·L-1盐酸,0.55 mol·L-1NaOH溶液,100 mL量筒2个 |
| C.0.50 mol·L-1盐酸,0.55 mol·L-1NaOH溶液,50 mL量筒1个 |
| D.0.50 mol·L-1盐酸,0.55 mol·L-1NaOH溶液,50 mL量筒2个 |
下列与化学反应能量变化相关的叙述正确的是( )
| A.生成物总能量一定低于反应物总能量 |
| B.等量H2在O2中完全燃烧,生成H2O(g)与生成H2O(l)放出的能量相同 |
| C.应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| D.同温同压下,H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件下的ΔH不同 |
下列说法错误的是( )
| A.热化学方程式未注明温度和压强时,ΔH表示标准状况下的数据 |
| B.热化学方程式中各物质前的化学计量数不表示分子个数,只代表物质的量 |
| C.同一化学反应,化学计量数不同,ΔH不同;化学计量数相同而状态不同,ΔH也不相同 |
| D.化学反应过程所吸收或放出的热量与参加反应的物质的物质的量成正比 |