下列反应属于吸热反应的是 ( )
| A.C6H12O6(葡萄糖aq)+6O2 ="" 6CO2+6H2O |
| B.CH3COOH+KOH = CH3COOK+H2O |
| C.A+B =C+D;△H<0 |
| D.破坏生成物全部化学键所需能量小于破坏反应物全部化学键所需能量 |
我国科研人员以蹄叶橐吾为原料先制得化合物Ⅰ,再转化为具有抗癌抑菌活性的倍半萜化合物Ⅱ,有关转化如图所示。下列有关说法不正确的是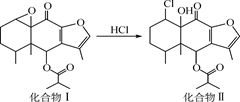
| A.化合物Ⅰ能使酸性KMnO4溶液褪色 |
| B.化合物Ⅰ分子中含有4个手性碳原子 |
| C.化合物Ⅱ一定条件下能发生取代、消去及加成反应 |
| D.检验化合物Ⅱ是否含化合物Ⅰ可用Br2的CCl4溶液 |
下列有关物质的性质和该性质的应用均正确的是
| A.浓硫酸具有吸水性,可用于干燥氨气、二氧化碳等气体 |
| B.二氧化硫具有漂白性,可用于加工食品使食品增白 |
| C.铝具有良好的导电性,钢抗拉强度大,钢芯铝绞线可用作远距离高压输电线材料 |
| D.铜的金属活动性比铁弱,可用铜罐代替铁罐贮运浓硝酸 |
常温下,用0.1000mol/L的NaOH溶液滴定20ml同浓度的一元弱酸HA,滴定过程溶液pH随X的变化曲线如图所示(忽略中和热效应),下列说法不正确的是
A.HA溶液加水稀释后,溶液中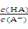 的值减小 的值减小 |
B.HA的电离常数 (x为滴定分数) (x为滴定分数) |
| C.当滴定分数为100时,溶液中水的电离程度最大 |
| D.滴定分数大于100时,溶液中离子浓度关系一定是c(Na+)>c(A-)>c(OH-)>c(H+) |
已知重铬酸钾(K2Cr2O7)溶液中存在如下平衡:Cr2O72-(橙色)+ H2O 2H++ 2CrO42-(黄色),①向2 mL 0.1 mol·L-1 K2Cr2O7溶液中滴入3滴6 mol·L-1 NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓H2SO4,溶液由黄色变为橙色。②向2 mL 0.1 mol·L-1酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,溶液由橙色变为绿色,发生反应:Cr2O72- + 14H++ 6Fe2+
2H++ 2CrO42-(黄色),①向2 mL 0.1 mol·L-1 K2Cr2O7溶液中滴入3滴6 mol·L-1 NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓H2SO4,溶液由黄色变为橙色。②向2 mL 0.1 mol·L-1酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,溶液由橙色变为绿色,发生反应:Cr2O72- + 14H++ 6Fe2+ 2Cr3+(绿色) + 6Fe3+ + 7H2O。下列分析正确的是
2Cr3+(绿色) + 6Fe3+ + 7H2O。下列分析正确的是
| A.实验①和②均能证明K2Cr2O7溶液中存在上述平衡 |
| B.实验②能说明氧化性:Cr2O72-> Fe3+ |
| C.CrO42-和Fe2+在酸性溶液中可以大量共存 |
| D.稀释K2Cr2O7溶液时,溶液中各离子浓度均减小 |
酚酞是中学阶段常用的酸碱指示剂,已知的结构简式如图所示:下列关于酚酞的说法正确的是
| A.酚酞属于芳香烃 |
| B.酚酞的分子式为C20H12O4 |
| C.酚酞结构中含有羟基(-OH),故酚酞属于醇 |
| D.酚酞在碱性条件下能够发生水解反应 |