已知氯水中有如下平衡:Cl2+H2O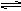 HCl+HclO。
HCl+HclO。
①常温下,在一个体积为50mL的针筒里吸入40mLCl2后,再吸进10mL水,写出针筒中可能观察到的现象是: 。
②若将此针筒长时间放置,又可能看到变化为: 。
试用平衡移动的观点加以解释: 。
(I)多项选择题
下列关于水处理的说法正确的是。
| A.FeSO4·7H2O是常用的混凝剂,它除去悬浮固体颗粒的过程只是物理过程 |
| B.用纯碱和生石灰处理硬水,既可以除去暂时硬度,也可以除去永久硬度 |
| C.永久硬度的水可以采用离子交换法进行软化,其主要就是利用了离子交换膜技术 |
| D.污水处理中的三级处理是采用化学方法,对污水进行深度处理和净化 |
E.电 渗析法是一种常用的海水淡化的方法,使用到的离子交换膜只有阳离子交换膜
渗析法是一种常用的海水淡化的方法,使用到的离子交换膜只有阳离子交换膜
(II)
下列是工业合成氨的简要流程示意图:
请回答下列问题:
(1)H2通常用碳氢化合物与水反应,写出有关的反应方程式,从冷凝器回流到压缩机中的X是。
(2)比较工业上合成氨和SO2的催化氧化反应,其生产条件有哪些异同,并解释原因
。
(3)将N2、H2按体积比1∶3进入合成塔,从合成塔出来的混合气中,氨的体积分数为15%,则H2的体积分数为______________。
(4)NH3的用途之一是制造化肥,但在化肥的使用过程中要注意铵态氮肥不可以和草木灰混用,解释其原因。
(5)NH3是一种重要的化工原料,除了制造化肥之外,再列举出两种NH3的用途
。
(I)多项选择题
下列说法中正确的是。
| A.SO2和O3、PO43—和C1O4—互为等电子体 |
| B.甲烷分子失去一个H+,形成CH3—,其碳原子的杂化类型发生了改变 |
| C.Ti原子的核外电子排布式为[Ar]3d34s2 |
| D.CS2、H2O、C2H2都是直线型分子 |
E.CH4、BCl3、CO2都是含有极性键的非极性分子
(II)
立方氮化硼 是一种自然界不存在的人工合成超硬材料,硬度仅次于金刚石,是超硬材料领域的最重要成就之一。请回答下列问题:
是一种自然界不存在的人工合成超硬材料,硬度仅次于金刚石,是超硬材料领域的最重要成就之一。请回答下列问题:
(1)在第二周期,原子的第一电离能一般随核电荷数的增大而逐渐,比较下列原子的第一电离能:Be B,N O(填“>”“<”),其原因是。
(2)下图为立方氮化硼的晶胞,则氮化硼的化学式为,该晶体中B原子填充N原子的空隙。若该晶胞的边长为a cm,那么该晶体的密度为g/cm3
(只要求列出算式)。
(3)立方氮化硼的晶体结构与金刚石的结构相似,但其熔点比金刚石的低,试分析其原因
。
(4)立方氮化硼由六方氮化硼在高温高压下制备,六方氮化硼又称“白石墨”,结构和许多性质与石墨相似,六方氮化硼中N原子的杂化轨道类型为,请在上方的方框中画出六方氮化硼的平面结构示意图(用“○”代表N原子,用“●”代表B原子,每种原子不少于7个)。
(I)多项选择题
在一定条件下,烯烃可发生臭氧氧化还原水解反应,生成羰基化合物,该反应可表示为:
 已知某有机物发生臭氧氧化还原水解反应后的产物为 CH3COCH2
已知某有机物发生臭氧氧化还原水解反应后的产物为 CH3COCH2 CHO,则该有机物可能是。
CHO,则该有机物可能是。
(II)
A~G都是有机化合物,它们的转化关系如下:
请回答下列问题:
(1)已知:有机物G的蒸气与甲烷的相对密度为11,取0.1mol的G完全燃烧生成48.4gCO2和10.8gH2O,则G的分子式是;
(2)写出B的结构简式;
(3)上述反应中属于取代反应的是(填代号);
(4)由E生成F的反应条件是;
(5)由C生成D的化学方程式是;
(6)同时满足下列两个条件的E的同分异构体共有 种,其中苯环上的一氯代物有两种同分异构体的是(填结构简式)。
种,其中苯环上的一氯代物有两种同分异构体的是(填结构简式)。
①分子内除了苯环外无其他环状结构,且苯环上有2个取代基;
②1mol该同分异构体与NaOH溶液反应时,可消耗3mol的NaOH。
A、B、C均为有机物,且 1mol B与碳酸氢钠反应生成2mol的二氧化碳。A、B、C有如图所示的转化关系:
试回答:
(1)写出A的结构简式________________________;
(2)写出B与C按物质的量之比1:1反应生成D的化学方程式_____________________,反应类型为;
(3)写出C3O2的结构式。
由短周期元素组成的X、Y、Z、M是中学化学常见的四种物质,它们有如图所示的转化关系,请根据题意回答问题。
(1)若X、Y、Z含有同种常见金属元素,M是O2。X为___________;Z与氢气在一定条件下化合生成一种产物,写出该反应的化学方程式________。
(2)若X、Y、Z含有同种常见非金属元素,气体Z能使品红溶液褪色。
①X的电子式为__________________ _______;
_______;
②Z与过量的氢氧化钠溶液反应的离子方程式是:_____________________________。
(3)若X的水溶液显碱性,X、M 均为气体,上述转化过程均在水溶液中进行。任写一个满足上述转化过程Y→Z反应的化学方程式______________________。
均为气体,上述转化过程均在水溶液中进行。任写一个满足上述转化过程Y→Z反应的化学方程式______________________。