把锌片和铁片放在盛有含酚酞的稀食盐水的玻璃器皿中,如图。经过一段时间后,首先观察到溶液变红的区域是()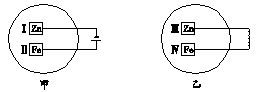
| A.Ⅰ和Ⅲ附近 | B.Ⅰ和Ⅳ附近 | C.Ⅱ和Ⅲ附近 | D.Ⅱ和Ⅳ附近 |
用NA表示阿伏加德罗常数的值,下列说法正确的是
| A.常温常压下,48 g O3含有的氧原子数约为3NA |
| B.常温常压下,11.2 L乙烯(C2H4)含有2NA个碳原子 |
| C.1.7 g氨气所含有的电子数目为10 NA |
| D.2.7g铝与足量氢氧化钠溶液反应转移的电子数NA |
国家质检总局调查结果显示:所谓毒奶粉是被三聚氰胺所污染,它可由三聚氰酸[C3N3(OH)3]制备.三聚氰酸可用于消除汽车尾气中的NO2,已知三聚氰酸中氮元素的化合价为-3价,HCNO中N为-3价,O为-2价,有关反应原理为:
① C3N3(OH)3 3HCNO;② 8HCNO+6NO2
3HCNO;② 8HCNO+6NO2 7N2+8CO2+4H2O
7N2+8CO2+4H2O
下列说法正确的是
| A.反应①中的两种物质互为同素异形体 | B.反应②中HCNO是氧化剂 |
| C.反应②中NO2是还原剂 | D.反应②中转移的电子数为24 |
关于化学反应中的说法错误的是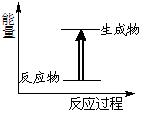
| A.化学键断裂吸收能量,化学键生成放出能量 |
| B.化学反应中有物质变化也有能量变化 |
| C.右图所示的反应为放热反应 |
| D.需要加热的化学反应不一定是吸热反应 |
下列措施中,能减慢化学反应速率的是
| A.用MnO2作H2O2分解反应的催化剂 |
| B.把石灰石固体研细后与盐酸反应 |
| C.把盛有Cu和稀硝酸的试管浸泡在热水中 |
| D.用10%的H2SO4溶液代替30%的H2SO4溶液与锌粒反应 |
下列有机反应中,有一种反应类型与其他三种反应类型不同的是
A.CH3COOH+CH3CH2OH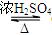 CH3COOCH2CH33+H2O CH3COOCH2CH33+H2O |
B.2CH3CH2OH+O2 2CH3CHO+2H2O 2CH3CHO+2H2O |
C.CH4+Cl2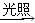 CH3Cl+HCl CH3Cl+HCl |
D.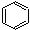 +Br2 +Br2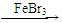 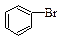 +HBr +HBr |