阿伏加德罗常数为6.02×1023mol-1,下列说法正确的是
| A.1 mol HClO完全分解时转移电子数为2×6.02×1023 |
| B.a L O2和N2的混合物中含有的分子数为a/22.4 ×6.02×1023 |
| C.100 mL 0.1 mol/L的Al2(SO4)3溶液中含有的Al3+数目为0.02×6.02×1023 |
| D.常温下,42 g C2H4和C4H8的混合物中含有的碳原子数为5×6.02×1023 |
下图为可逆反应A(g)+2B(g) nC(g)(正反应放热)生成物C的浓度随压强变化并建立平衡的关系图,则n值与压强p1、p2的关系正确的是
nC(g)(正反应放热)生成物C的浓度随压强变化并建立平衡的关系图,则n值与压强p1、p2的关系正确的是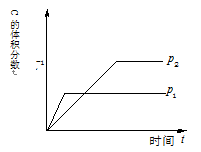
| A.p2>p1,n<3 |
| B.p2>p1,n>3 |
| C.p1>p2,n<3 |
| D.p1>p2,n>3 |
下列事实,不能用勒夏特列原理解释的是
A.在溴水中存在如下平衡:Br2+H2O HBr+HBrO,当加入NaOH溶液后颜色变浅 HBr+HBrO,当加入NaOH溶液后颜色变浅 |
B.合成氨反应:N2+3H2 2NH3 △H < 0,为使氨的产率提高,理论上应采取低温高压的措施 2NH3 △H < 0,为使氨的产率提高,理论上应采取低温高压的措施 |
C.反应CO+NO2 CO2+NO △H < 0升高温度使平衡向逆方向移动 CO2+NO △H < 0升高温度使平衡向逆方向移动 |
D.对2HI H2+I2(g)平衡体系增加压强使颜色变深 H2+I2(g)平衡体系增加压强使颜色变深 |
某温度时,浓度都是1mol·L-1的两种气体,X2、Y2在密闭容器中反应生成气体Z,达到平衡时c(X2)=0.4mol·L-1、c(Y2)=0.8mol·L-1、c(C)=0.4mol·L-1,则该反应的反应式是
A.X2+2Y2 XY2 B.2X2+Y2
XY2 B.2X2+Y2 2X2Y
2X2Y
C.3X2+Y2 2X3Y D.X2+3Y2
2X3Y D.X2+3Y2 2XY3
2XY3
对反应4A+5B 4C+6D,以下化学反应速率的表示中,所表示反应速率最快的
4C+6D,以下化学反应速率的表示中,所表示反应速率最快的
A.v (A)=0.40mol•L-1•s-1 B.v (B)=0.48mol•L-1•s-1
C.v (C)=0.36mol•L-1•s-1 D.v (D)=0.55mol•L-1•s-1
反应4A(s)+3B(g) 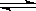 2C(g)+D(g),经2min,B的浓度减少0.6 mol•L-1。对此反应速率的表示,正确的是
2C(g)+D(g),经2min,B的浓度减少0.6 mol•L-1。对此反应速率的表示,正确的是
①用A表示的反应速率是0.4 mol•L-1•min-1
②分别用B、C、D表示的反应速率其比值为3:2:1
③在2 min末的反应速率,用B表示是0.3 mol•L-1•min-1
④反应的过程中,只增加A的量,反应速率不变
A.①② B.③ C.① D.②④