下列离子方程式书写正确的是
| A.向碳酸氢钙溶液中加入足量氨水:Ca2++2HCO3-+2OH-="==" CaCO3↓+CO32-+2H2O |
| B.向KI与稀硫酸的混合溶液中通入氧气:4H++O2+4I-===2I2+2H2O |
| C.次氯酸钠溶液中通入二氧化硫气体:2ClO-+SO2+H2O=2HClO+SO32- |
D.硫化钠的水解反应:S2-+H3O+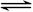 HS-+H2O HS-+H2O |
对于在一定条件下进行的化学反应:2SO2+O2 2SO3,改变下列条件,可以提高反应物中的活化分子百分数的是
2SO3,改变下列条件,可以提高反应物中的活化分子百分数的是
| A.升高温度 | B.增大压强 | C.压缩使容器体积变小 | D.增大反应物浓度 |
下列说法中正确的是
| A.非自发反应在任何条件下都不能实现 |
| B.自发反应一定是熵增大,非自发反应一定是熵减小或不变 |
| C.凡是放热反应都是自发的,吸热反应都是非自发的 |
| D.熵增加且放热的反应一定是自发反应 |
下列反应既属于氧化还原反应,又是吸热反应的是
| A.铝片与盐酸的反应 | B.灼热的碳与CO2的反应 |
C.Ba(OH)2·8H2 O与NH4Cl固体的反应 O与NH4Cl固体的反应 |
D.甲烷在氧气中的燃烧反应 |
下列反应既属于氧化还原反应,又是吸热反应的是
| A.锌粒与稀硫酸的反应 | B.灼热的木炭与CO2反应 |
| C.甲烷在氧气中的燃烧反应 | D.Ba(OH)2·8H2O晶体与NH4Cl晶体的反 |
A、B、C均为短周期元素,它们在周期表中的位置如右图.已知B、C两元素在周期表中族序数之和是A元素族序数的2倍;B、C元素的原子序数之和是A元素原子序数的4倍,则A、B、C 所在的一组是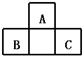
A.Be、Na、Al B.B、Mg、Si C.O、P、Cl D. C、Al、P