某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应A(g)+xB(g)  2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的如下图所示。下列说法中正确是
2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的如下图所示。下列说法中正确是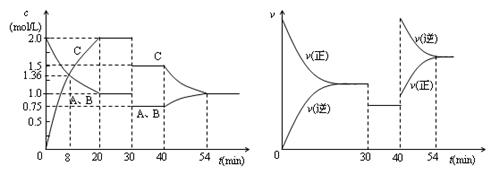
| A.30min时降低温度,40min时升高温度 |
| B.8min前A的平均反应速率为0.08mol/(L·min) |
| C.反应方程式中的x=1,正反应为吸热反应 |
| D.20min~40min间该反应的平衡常数均为4 |
某溶液中滴入BaCl2溶液,产生白色沉淀,再滴入稀硝酸,沉淀不溶解,则该溶液中:
| A.一定有SO2-4 | B.SO2-4、SO2-3或Ag+中至少有一种 |
| C.一定无Ag+ | D.可能有CO2-3 |
下列关于电解质、非电解质的说法正确的是
| A.氯气溶于水得氯水,该溶液能导电,因此氯气是电解质 |
| B.CaCO3饱和溶液导电能力很弱,故CaCO3是弱电解质 |
| C.导电能力弱的溶液肯定是弱电解质的溶液 |
| D.HF的水溶液中既有H+、F-,又有大量的HF分子,因此HF是弱电解质 |
NA表示阿伏加德罗常数,下列说法正确的是:
| A.2 mol·L-1的Na2SO4溶液中含有4NA个Na+ |
| B.18克水所含的电子数为10NA |
| C.在标准状况下,11.2L氖气中含有NA个氖原子 |
| D.NA个水分子的相对分子质量之和等于水的摩尔质量 |
按照物质的树状分类和交叉分类,HNO3应属于:①酸 ②氢化物 ③氧化物 ④含氧酸 ⑤难挥发性酸 ⑥强氧化性酸 ⑦一元酸 ⑧化合物 ⑨混合物
| A.①②③④⑤⑥⑦⑧ | B.①④⑥⑦⑧ | C.①⑨ | D.①④⑤⑥⑦ |
实验室从碘水中得到纯净的碘的操作,正确的是:
| A.分液、蒸馏 | B.过滤、蒸发 | C.萃取、分液 | D.萃取、分液、蒸馏 |