亚硫酰氯(SOCl2)是重要的有机物卤化剂和电池的介质,生产上和生活中有着广泛应用,亚硫酰氯易水解,在140℃以上可发生:4SOCl2=3Cl2↑+2SO2↑+S2Cl2。有关说法不正确的是
| A.1mol SOCl2受热分解,转移2mol电子 |
| B.S2Cl2分子中各原子均达到八电子结构 |
| C.气态产物通入品红溶液中,一定能使品红溶液褪色 |
| D.工业上用ZnCl2·6H2O与SOCl2混合制无水氯化镁,是利用SOCl2水解释放出HCl, |
抑制氯化锌的水解
下列与实验相关的叙述正确的是
| A.Hg(NO3)2 溶于水,可将含有Hg(NO3)2 的废液倒入水池中,再用水冲入下水道 |
| B.用蒸发方法使NaCl 从溶液中析出时,应将蒸发皿中NaCl 溶液全部蒸干才停止加热 |
| C.用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,必须冷却至室温才能转移到容量瓶中 |
| D.分液操作时,下层液体从分液漏斗下口放出,上层液体从下口放出到另一个烧杯 |
下列除杂所选用的试剂及操作方法均正确的一组是(括号内为杂质)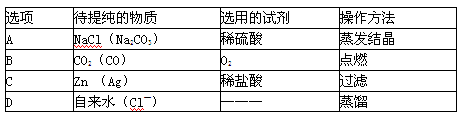
下列离子方程式书写正确的是
| A.碳酸氢钠与稀硫酸反应:CO32— + 2H+= CO2↑ + H2O |
| B.澄清石灰水跟稀硝酸反应:H++OH— = H2O |
| C.氧化镁与醋酸反应:MgO+2H+=Mg2++H2O |
| D.盐酸滴到铜片上:Cu+2H+ = Cu2++H2↑ |
下列溶液中Cl-物质的量浓度最大的是
| A.200mL 2mol/L MgCl2溶液 | B.1000mL 2.5mol/L NaCl溶液 |
| C.300mL 5mol/L KClO3溶液 | D.250mL 1mol/L AlCl3溶液 |
下列四种物质的溶液,其中一种与其它三种能发生离子反应,这种物质是
| A.BaCl2 | B.KOH | C.H2SO4 | D.Na2CO3 |