PCl5是一种白色固体,加热到160℃不经过液态阶段就变成蒸气,测得180℃下的蒸气密度(折合成标准状况)为9.3g/L, 极性为零,P—Cl键长为204pm和211pm两种。继续加热到250℃时测得压力为计算值的两倍。PCl5在加压下于148℃液化,形成一种能导电的熔体,测得P—Cl的键长为198pm和206pm两种。(P、Cl相对原子质量为31.0、35.5)回答如下问题:(1)180℃下PCl5蒸气中存在什么分子?为什么?写出分子式,画出立体结构。(2)在250℃下PCl5蒸气中存在什么分子?为什么?写出分子式,画出立体结构。(3)PCl5熔体为什么能导电?用最简洁的方式作出解释。(4) PBr5气态分子结构与PCl5相似,它的熔体也能导电,但经测定其中只存在一种P-Br键长。PBr5熔体为什么导电?用最简洁的形式作出解释。
(7分)燃烧法是测定有机化合物化学式的一种重要方法。现在完全燃烧0.1 mol某烃,燃烧产物依次通过右图所示的装置,实验结束后,称得甲装置增重10.8 g,乙装置增重11.2 g。求该烃的分子式,并写出其所有同分异构体的结构简式。
将等物质的量的A、B混合于2 L的密闭容器中,发生反应:3A(g)+B(g) xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率是0.1 mol/(L·min)。求:
xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率是0.1 mol/(L·min)。求:
(1)反应开始前放入容器中的A、B的物质的量;
(2)x的值;
(3)B的平均反应速率。
将等物质的量的A、B、C、D四种物质混合放入V L密闭容器中,发生如下反应:aA+bB cC(s)+dD,当反应进行到第t min时,测得A减少了n mol,B减少了
cC(s)+dD,当反应进行到第t min时,测得A减少了n mol,B减少了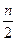 mol,C增加了
mol,C增加了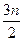 mol,D增加了n mol。此时反应达到平衡。
mol,D增加了n mol。此时反应达到平衡。
(1)该化学方程式中,各物质的化学计量数分别为:a=__________、b=__________、c=__________、d=__________。
(2)以B的浓度变化表示的该化学反应的速率为v(B)=______________________________。
(3)若只改变压强,反应速率发生变化,但平衡不发生移动,该反应中各物质的聚集状态是:A__________、B__________、D__________。
(4)若只升高温度,反应一段时间后,测知四种物质的物质的量又达到相等,则该反应为__________反应。(填“放热”或“吸热”)
在容积为2 L的密闭容器中充入1 mol A和2 mol B,按2A(g)+B(g) 3C(g)进行反应,经4 min后,测得C的物质的量为0.6 mol,试计算分别用A、B、C三种不同物质表示的该反应的反应速率。
3C(g)进行反应,经4 min后,测得C的物质的量为0.6 mol,试计算分别用A、B、C三种不同物质表示的该反应的反应速率。
(5分)把铝、铁混合物1.1 g溶于200 mL 5 mol·L-1盐酸中,反应后盐酸的浓度变为4.6 mol·L-1(溶液体积变化忽略不计)。
求:(1)反应中消耗HCl的物质的量。
(2)该混合物中铝、铁的物质的量。