某课外活动小组利用如图所示装置分别做如下实验:
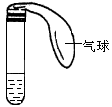
①在试管中注入某红色溶液,加热试管,溶液颜色变浅,冷却后
恢复红色,则原溶液可能是________________溶液;加热时溶液由红色逐渐变浅的原因是:_________________________。②在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复无色, 则此溶液可能是_____________溶液;加热时溶液由无色变为红色的原因是:__________________________________。
某研究性学习小组的同学利用下列装置进行乙醇催化氧化的实验。请分析回答:
(1)请写出实验过程中的总的化学反应方程式__________________________。
(2)在不断鼓入空气的情况下,移去酒精灯,反应仍能继续进行,说明乙醇的催化氧化反应是________反应。进一步研究表明,鼓气速度与反应体系的温度关系曲线如右图所示。鼓气速度过快,反应体系温度反而下降的原因___________________________。
(3)甲和乙两个水浴作用不相同。
甲的作用是________________;乙的作用是_________________________。
(4)反应进行一段时间后,干燥试管a中能收集到不同的物质,它们是___________。集气瓶中收集到的气体的主要成分是_______________。
(5)在检验生成物的过程中,一位同学很偶然地发现向溴水中加入乙醛溶液,溴水褪色。针对溴水褪色的原因,该小组的同学们经过分析后,提出两种猜想:
①溴水将乙醛氧化为乙酸;②溴水与乙醛发生加成反应。
请你设计一个简单的实验,探究哪一种猜想正确?_______________________。
某化学课外活动小组欲制取纯碱Na2CO3溶液并讨论实验过程中的相关问题。可供选择的试剂有:A大理石;B盐酸;C氢氧化钠溶液;D澄清石灰水。
三名同学设计的制备方案的反应流程分别如下: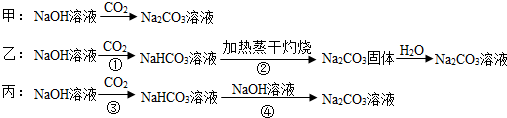
(1)请指出甲、乙两方案的主要缺点:
甲方案_______________________;
乙方案_______________________;
(2)若采用丙方案制取纯Na2CO3溶液,其实验的关键有______________________;
(3)假设反应②所得的Na2CO3固体中混有未分解的NaHCO3.乙同学选择澄清石灰水测定其中NaHCO3的质量分数,乙同学能否达到实验目的? ______________(填“能”或“不能”)若能,请说明其计算所需的数据;若不能,请简要说明理由______________。
三氯化碘(ICl3,I的化合价为+3价)在药物合成中用途广泛,其熔点:33℃,沸点:73℃,实验室可用如图装置制取ICl3。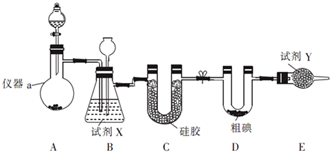
(1)制备氯气选用的药品为漂白精固体(主要成分为Ca(ClO)2)和浓盐酸,相关反应的化学方程式为:____________________________;
试剂X为________________、Y为______________;
(2)装置B可用于除杂,也是安全瓶,能监测实验进行时装置C中是否发生堵塞,请写出发生堵塞时B中的现象____________________________;
(3)某同学欲测定ICl3样品中ICl3的纯度,他准确称取ICl3样品10.0g于烧杯中,加入适量水和过量KI晶体,充分反应:ICl3+3KI═2I2+3KCl(样品中杂质不反应).将所得溶液配置成100mL待测液.取25.00mL待测液,用2.0mol/L的Na2S2O3标准液滴定(I2+2S2O32-═2I-+S4O62-),以淀粉溶液作指示剂,达到终点时的现象为____________________________;重复滴定,实验数据记录如下:
| 滴定次数 |
待测液体积/mL |
Na2S2O3标准液体积/mL |
|
| 滴定前读数(mL) |
滴定后读数(mL) |
||
| 第一次 |
25.00 |
0.50 |
20.40 |
| 第二次 |
25.00 |
4.00 |
24.10 |
| 第三次 |
25.00 |
4.20 |
26.70 |
该样品中ICl3的质量分数为_______________(ICl3相对分子质量为233.5)
浅绿色的硫酸亚铁铵晶体[又名莫尔盐,(NH4)2SO4·FeSO4·6H2O]比绿矾(FeSO4·7H2O)更稳定,常用于定量分析。莫尔盐的一种实验室制法如下: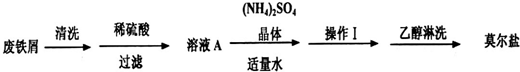
(1)向废铁屑中加入稀硫酸后,并不等铁屑完全溶解而是剩余少量时就进行过滤,其目的是_________;
(2)浓度均为0.10mol•L-1的莫尔盐溶液和FeSO4溶液,c(Fe2+)前者______后者.(填“大于”、“小于”或“等于”或“无法判断”)
(3)0.10mol•L-1莫尔盐溶液中离子浓度由大到小的顺序为_________;
(4)常温下,若0.10mol•L-1(NH4)2SO4溶液的pH=5,求算NH3•H2O的电离平衡常数Kb≈________;
实验室中欲配制225mL6 mol•L-1的H2SO4溶液,现有足量的18mol•L-1的浓硫酸。现有三种规格容量瓶:100mL、250 mL、500 mL,试回答:
(1)此时最少需要________ mL 浓H2SO4.
(2)可供选择的仪器除容量瓶外,还有 ①玻璃棒②烧瓶③烧杯④量筒⑤药匙 ⑥托盘天平.
上述仪器中,在配制6mol/L 的H2SO4时用不到的仪器是(填代号)________,缺少的仪器是________,你选择的容量瓶的规格是________ mL。使用容量瓶(已经洗涤干净)时的第一步操作是________;
(3)用量筒量取浓硫酸后,应如何混合稀释浓硫酸________;
(4)在配制过程中,下列操作中错误________,能导致结果偏低的操作是________,(填代号,其他操作都正确)。
| A.洗涤量取浓H2SO4后的量筒2-3次,并将洗涤液转移到容量瓶中 |
| B.先将浓H2SO4沿着烧杯壁慢慢到入烧杯中,再向烧杯中加入蒸馏水来稀释 |
| C.未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中 |
| D.定容时,加蒸馏水超过容量瓶刻度,又用胶头滴管吸出 |
E.转移溶液前,容量瓶中含有少量蒸馏水
F.定容摇匀后,发现液面低于刻度,又用胶头滴管加蒸馏水至刻度