将5.4 g Al投入到200.0 mL 2.0 mol·L-1的某溶液中有氢气产生,充分反应后有金属剩余。该溶液可能为( )
| A.HNO3溶液 | B.Ba(OH)2溶液 |
| C.H2SO4溶液 | D.HCl溶液 |
以下性质的比较中,不正确的是
| A.晶格能 NaCl<MgO |
| B.熔点:NH3<PH3 |
| C.离子半径:Na+<O2- |
| D.第一电离能:Mg>Al |
下列四种分子中中心原子杂化类型与三个不同的是
| A.CH4 | B.NH3 | C.H2O | D.BF3 |
下列说法正确的是
| A.晶体在受热熔化过程中一定存在化学键的断裂 |
| B.原子晶体的原子间只存在共价键,而分子晶体内只存在范德华力 |
| C.区分晶体和非晶体最科学的方法是对固体进行X-射线衍射实验 |
| D.非金属元素的原子间只形成共价键,金属元素的原子非金属元素的原子间只形成离子键 |
在体积为1 L的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:
CO2(g)+3H2(g)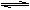 CH3OH(g)+H2O(g) △H=-49.0kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如图所示。下列说法正确的是
CH3OH(g)+H2O(g) △H=-49.0kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如图所示。下列说法正确的是
| A.从反应开始到平衡,氢气的平均反应速率为0.225mol/(L·min) |
| B.图中交点表示反应达到化学平衡状态 |
| C.升高温度,n(CH3OH)/n(CO2)减小 |
| D.10分钟后向容器再充入1mol CO2和3mol H2,重新达平衡后,CO2体积分数将增大 |
Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如下,电解总反应:2Cu+H2O Cu2O+H2
Cu2O+H2 。下列说法正确的是
。下列说法正确的是
| A.石墨电极上产生氢气 |
| B.铜电极发生还原反应 |
| C.电解过程中电子从电源正极流出经导线流向铜极 |
| D.当有0.1mol电子转移时,有0.1molCu2O生成 |