下列各组离子反应可用H++OH-=H2O表示的是( )
| A.氢氧化钡和硫酸 | B.氢氧化铁和盐酸 |
| C.硝酸和氢氧化钠 | D.硫酸氢钠和氢氧化钠 |
向Ba(OH)2和NaOH混合溶液中缓缓通入CO2气体至过量,生成沉淀物质的量与通入CO2气体的体积V(标准状况)的关系如图所示,下列结论不正确的是
A.原混合物中n[Ba(OH)2] n [NaOH]=1:2 n [NaOH]=1:2 |
| B.横坐标轴上p点的值为90 |
| C.b点时溶质为NaHCO3 |
D.ab段发生反应的离子方程式依次为:CO2+2OH-→ H2O+CO32-,CO2 H2O+ CO32-→2HCO3- H2O+ CO32-→2HCO3- |
一定量的乙醇在氧气不足的情况下燃烧,得到CO、CO2和水的总质量为27.2g,若其中水的质量为10.8g。则CO的质量是
| A.2.1g | B.2.6g | C.3.8g | D.5.1g |
向AgCl浊液中滴加氨水后可得到澄清溶液,继续滴加浓硝酸后又有沉淀生成。经查资料得知:Ag++2NH3 H2O
H2O [Ag(NH3)2]
[Ag(NH3)2] +2H2O。下列分析不正确的是
+2H2O。下列分析不正确的是
A.浊液中存在沉淀溶解平衡:AgCl(s) Ag+ (aq) Ag+ (aq) Cl-(aq) Cl-(aq) |
| B.实验可以证明NH3结合Ag+能力比Cl-强 |
| C.实验表明实验室可用氨水洗涤银镜反应后的试管 |
| D.由资料信息可推知:加浓硝酸后生成的沉淀为AgCl |
pC类似pH,是指稀溶液中溶质物质的量浓度的负对数。如某溶液溶质的浓度为1×10-3mol/L,则该溶液中溶质的pC=3。下列叙述正确的是
A.某温度下,任何电解质的稀溶液中,pC(H+)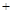 pC(OH-) pC(OH-) |
| B.0.01mol/L的CaCl2溶液中逐滴加入纯碱溶液,滴加过程中pC(Ca2+)逐渐增大 |
C.0.01mol/L的BaCl2溶液中,pC(Cl-) 2pC(Ba2+) 2pC(Ba2+) |
| D.用0.01mol/L的盐酸滴定某浓度的NaOH溶液,NaOH溶液的pC(OH-)逐渐减小 |
从海带中提取碘,可经过以下实验步骤完成。下列有关说法正确的是
| A.灼烧过程中使用的玻璃仪器有酒精灯、坩埚、玻璃棒 |
B.氧化过程中发生反应的离子方程式为:2I- H2O2 → I2 H2O2 → I2 2OH- 2OH- |
| C.检验碘单质时,可选用淀粉碘化钾试纸,若试纸变蓝说明有碘单质 |
| D.分液时,先打开活塞放出下层液体,再关闭活塞倒出上层液体 |