下列各组离子能在溶液中大量共存的是( )
A.K+、Ag+、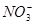 、Cl- 、Cl- |
B.Ba2+、Na+、 、OH- 、OH- |
C.Mg2+、Ba2+、OH-、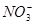 |
D.OH-、K+、 、 、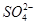 |
分子式为 C7H8的苯的同系物的一氯代物的种类有( )
| A.1种 | B.2种 | C.3种 | D.4种 |
下列各组有机物中,只需加入溴水就能一一鉴别的是( )
| A.已烯、苯、 四氯化碳 |
| B.已炔、己烯、四氯化碳 |
| C.已烷、苯、乙醇 |
| D.甲苯、苯、已烯 |
下列反应中属于加成反应的是( )
| A.乙炔通入酸性高锰酸钾溶液中,溶液褪色。 |
| B.苯滴入溴水中,振荡后溴水层接近无色。 |
| C.甲烷和氯气混合后,放置在光亮的地方,混合气体颜色逐渐变浅 |
| D.将裂化获得的汽油滴入溴水中,溴水褪色 |
某烃的结构简式为: -C≡C-CH=CH-CH3,有关其结构说法正确的是( )
-C≡C-CH=CH-CH3,有关其结构说法正确的是( )
| A.所有原子可能在同一平面上 |
| B.所有碳原子可能在同一平面上 |
| C.所有原子可能在同一条直线上 |
| D.所有氢原子可能在同一平面上 |
若是某单炔烃与氢气加成后的产物 ,则炔烃的结构可能有()
,则炔烃的结构可能有()
| A.2种 | B.3种 | C.4种 | D.5种 |