将金属与金属(或非金属)加热熔合在一起就能形成合金。根据下列金属的熔点、沸点:
| Na |
Cu |
Al |
Fe |
|
| 熔点/℃ |
97.81 |
1 083 |
660 |
1 535 |
| 沸点/℃ |
882.9 |
2 595 |
2 467 |
3 000 |
其中不能形成合金的是( )
| A.Fe、Cu | B.Al、Na | C.Fe、Na | D.Cu、Na |
高温下用CO还原m gR2O2得n gR,已知氧的相对原子质量为16,则R的相对原子质量是( )
A.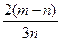 |
B.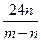 |
C.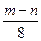 |
D.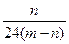 |
在同温同压下,40 mL气体A2与120 mL气体B2恰好完全反应生成80 mL气体X,则气体X的化学式为()
| A.AB3 | B.AB | C.A3B | D.A2B3 |
某温度下,将Cl2通入氢氧化钾溶液中,反应后得到KCl、KClO、KClO3的混合溶液,经测定ClO-与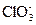 的物质的量之比为1∶2,则Cl2与KOH反应时,被还原的氯原子与被氧化的氯原子的物质的量之比为()
的物质的量之比为1∶2,则Cl2与KOH反应时,被还原的氯原子与被氧化的氯原子的物质的量之比为()
| A.2∶3 | B.4∶3 | C.10∶3 | D.11∶3 |
反应A+3B 2C,若7 g A和一定量B完全反应生成8.5 g C,则A、B、C的相对分子质量之比为()
2C,若7 g A和一定量B完全反应生成8.5 g C,则A、B、C的相对分子质量之比为()
A.14∶3∶17 B.28∶2∶17
C.1∶3∶2 D.无法确定
在标准状况下,足量MnO2氧化了100 mL的浓盐酸,生成Cl2体积为3.36 L,该盐酸物质的量浓度是()
| A.3 mol·L-1 | B.0.3 mol·L-1 |
| C.6 mol·L-1 | D.0.6 mol·L-1 |