某化学兴趣小组按照下列方案进行“由含铁废铝制备硫酸铝晶体”的实验:
步骤1:取一定量含铁废铝,加足量的NaOH溶液,反应完全后过滤。
步骤2:边搅拌边向溶液中滴加稀硫酸至溶液pH=8~9,静置、过滤、洗涤。
步骤3:将步骤2中得到的固体溶于足量的稀硫酸。
步骤4:将得到的溶液范发浓缩、冷却、结晶、过滤、干燥。
请回答以下问题:
(1)上述实验中的过滤操作需要玻璃棒、_______、_______等玻璃仪器。
(2)步骤1过滤的目的是______________。
(3)当步骤2中溶液的pH=8~9时,检验沉淀是否完全的方法是______________。
(4)步骤2中溶液的pH较难控制,可改用_______。
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应。应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”。请回答该实验中的问题。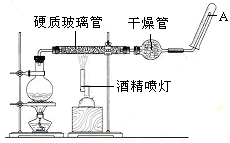
(1)写出该反应的化学方程式,其中氧化剂是,还原剂是。8.4g铁粉参加反应,转移电子mol。
(2)玻璃管中石棉绒的作用是,实验开始时应先点燃,实验结束时应先熄灭。
(3)圆底烧瓶中盛装的水,该装置受热后的主要作用是;烧瓶里应事先放置,其作用是。
(4)该同学欲确定反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红色则说明硬质试管中固体物质的成分是,若溶液未变红色则说明硬质试管中固体物质的成分是。
(5)该同学按上述实验方案进行了实验,结果溶液未变红色,原因是(用离子方程式表示)。
(6)该同学马上另取少量溶液B,使其跟NaOH溶液反应。若按图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出与上述现象相关的反应的化学方程式,。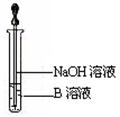
(7)一段时间后,该同学发现(4)中未变红的溶液变成红色,说明Fe2+ 具有性。由此可知,实验室中含Fe2+的盐溶液现用现配制的原因是,并且配制含Fe2+的盐溶液时应加入少量。
Ⅰ.选择下列实验方法分离物质,将分离方法的序号填在横线上。
| A.萃取分液 |
| B.升华 |
| C.结晶 |
| D.分液 |
E.蒸馏
F.层析
G.过滤
(1)______分离饱和食盐水与沙子的混合物。
(2)______从硝酸钾和氯化钠的混合液中获得硝酸钾。
(3)______分离水和汽油的混合物。
(4)______分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物。
Ⅱ.海带含有丰富的碘,为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
请填写下列空白:
(1)步骤①所需仪器除酒精灯、三脚架、泥三角外,还需要。
(2)步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤应选择的实验装置是。
(3)步骤④反应的离子方程式是。
(4)步骤⑤中,某学生选择用苯来提取碘的理由是________________________。
(5)请设计一个简单的实验方案,检验提取碘后的水溶液中是否还含有单质碘:。
利用硫酸厂烧渣(含铁的氧化物和少量FeS及SiO2)制碱式硫酸铁的流程如下:
(1)SO2与过量NaOH溶液反应的离子方程式为。
(2)滤渣的主要成分为(填化学式)。
(3)反应1中加双氧水的目的是。
(4)碱式硫酸铁的化学式为Fex(OH)y(SO4)z·nH2O,为确定其组成进行如下实验:
①称取1.6920 g 样品溶于足量的稀盐酸中;
②加足量的BaCl2溶液,过滤、洗涤、干燥、称重,得固体质量为2.3300 g;
③向步骤②的滤液中加过量的NaOH溶液,过滤、洗涤、灼烧、称重,得固体质量为0.6400 g。
根据以上实验数据计算碱式硫酸铁样品中的n(OH-): n(SO42-)(写出计算过程)
(10分)镁铝合金在交通、航空、电子等行业有着广泛的应用。某化学兴趣小组试对镁铝合金废料进行回收利用,实验中可将铝转化为硫酸铝晶体,并对硫酸铝晶体进行热重分析。镁铝合金废料转化为硫酸铝晶体实验流程如下: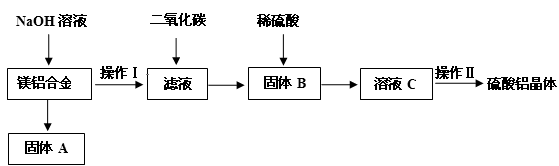
试回答下列问题:
(1)在镁铝合金中加入NaOH溶液,写出反应的化学反应方程式,固体B的化学式。
(2)操作Ⅱ包含的实验步骤有:蒸发浓缩、、、洗涤、干燥。
(3)操作Ⅱ中常用无水乙醇对晶体进行洗涤,选用无水乙醇的原因是。
(4)若初始时称取的镁铝合金废料的质量为9.00 g,得到固体A的质量为4.95 g,硫酸铝晶体的质量为49.95 g(假设每一步的转化率均为100%,合金废料中不含溶于碱的杂质)。计算得硫酸铝晶体的化学式为。
(5)取上述硫酸铝晶体进行热重分析,其热分解主要分为三个阶段:323K-523K,553K-687K,1043K以上不再失重,其热分解的TG曲线见下图,
已知: 。
。
根据图示数据计算确定每步分解的产物,写出第一阶段分解产物的化学式,第三阶段反应化学方程式。
用中各滴定法测定某烧碱样品的纯度,若烧碱中含有不反应的杂质,试根据实验回答:
(1)将准确称好的5.0 g烧碱样品配成250 mL待测液,需要的主要仪器除量筒、烧杯、玻璃棒、胶头滴管处,还必须用到的玻璃仪器有________。
(2)取待测液10.00 mL,需用________(填仪器名称)量取,并置于锥形瓶中。
(3)向锥形瓶中滴加两滴指示剂,用0.200 mol/L HCl溶液滴定烧碱溶液。不适宜选用的指示剂为(选序号填):________。
①石蕊溶液②酚酞溶液 ③甲基橙溶液
(4)滴定操作的要领是:左手握活塞,右手摇锥形瓶,眼睛要注视________。
(5)根据下表实验数据,可计算出烧碱的纯度为________。
| 滴定次数 |
待测液体积(mL) |
HCl溶液体积(mL) |
|
| 滴定前读数 |
滴定后读数 |
||
| 第一次 |
10.00 |
0.50 |
20.51 |
| 第二次 |
10.00 |
4.00 |
24.00 |
| 第三次 |
10.00 |
5.11 |
25.10 |
(6)下列操作会使所测溶液的浓度数值偏高的是(填代号)________。
A.酸式滴定管未用HCl溶液润洗就直接注入HCl溶液
B.锥形瓶用蒸馏水洗净后没有干燥就注入NaOH待测液
C.装有HCl溶液的酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取HCl溶液体积时,开始仰视读数,滴定结束后俯视读数