已知某主族金属元素X的原子核内质子数和中子数之比为1:1,含该金属阳离子0.192g的溶液恰好能将20mL0.4mol/L的Na2CO3溶液中的CO32-全部沉淀,推断X是什么元素及在周期表中的位置。
将等物质的量的两种氧化物溶于100 mL硫酸,而后逐滴加入1.00 mol·L-1的NaOH溶液。当加入的NaOH的体积V1="50" mL时,开始有沉淀析出,且沉淀量随NaOH加入量逐渐增加;当NaOH的体积V2="650" mL 时,沉淀量达最大值,继续滴加NaOH时,沉淀量逐渐减小;当V3≥750 mL时,沉淀量不再改变。
(1)最初加入的50 mL NaOH溶液的作用是什么?
答:__________________________________________。
(2)画出沉淀量(m)随NaOH溶液体积滴入量的变化关系,并计算所用硫酸的浓度。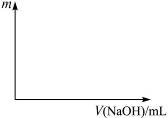
图4-5
(3)试判断两种氧化物各是什么,并计算其物质的量。
将一定质量的MgAl合金投入100 mL一定物质的量浓度的HCl中,合金全部溶解,向所得溶液中滴加5 mol·L-1 NaOH溶液至过量,生成的沉淀质量与加入的NaOH溶液的体积关系如图4-7所示。
图4-7
求:(1)原合金中Mg、Al质量各多少克。
(2)HCl物质的量浓度。
由铝和某种金属组成的混合物,将它分成质量相等的两份。一份放入过量的盐酸中,混合物全部作用完,放出H2 6.16 L(标准状况),溶液质量比反应前增加4.85 g;另一份放入过量烧碱溶液中,反应完毕后,放出H2 4.48 L(标准状况),溶液的质量比反应前增加3.2 g,而某金属则不反应,沉积出来。求:(1)原混合物中某金属的质量。
(2)某金属的相对原子质量。
在密闭容器中充入PCl5(g) PCl3(g)+Cl2(g),反应一段时间后又向体系中加入37Cl2含量较多的氯气,问在没有达平衡之前PCl3(g)中37Cl的含量是否会增加?为什么?
PCl3(g)+Cl2(g),反应一段时间后又向体系中加入37Cl2含量较多的氯气,问在没有达平衡之前PCl3(g)中37Cl的含量是否会增加?为什么?
某温度下在密闭容器中发生如下反应:
2M(g)+N(g) 2E(g)
2E(g)
开始时只充入2 mol E(g),达平衡时,混合气体的压强比起始时增大了20%。若开始时只充入2 mol M和1 mol N的混合气体,达平衡时M的转化率为多少?