下列叙述中正确的是
| A.实验室制取氨气的发生装置与用高锰酸钾制取氧气的装置相同 |
| B.并不是所有的铵盐都能与烧碱共热生成氨气 |
| C.除去NO中混有的少量NO2,可将混合气体通过盛有水的洗气瓶,再用排空气法收集NO |
| D.CO2、NO2、P2O5均与水反应生成酸为酸性氧化物 |
下列叙述正确的是
| A.将一小块铜片放入盛有浓硫酸的试管中加热反应后的溶液呈蓝色 |
| B.将一小块钠放入盛有水的烧杯中钠在水面上游动,同时看到烧杯内的溶液变为红色 |
C.如图,一段时间后给烧杯内的溶液中加入黄色的K3[Fe(CN)6]溶液,可看到电极附近有蓝色沉淀生成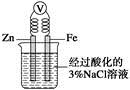 |
| D.向盛有少量Mg(OH)2沉淀悬浊液的试管中滴加氯化铵溶液,可看到沉淀溶解 |
下列实验操作正确的是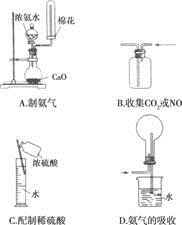
关于下列各实验装置的叙述中,正确的是
| A.装置①制备乙酸乙酯 |
| B.装置②中X若为CCl4,可用于吸收NH3或HCl,并防止倒吸 |
| C.装置③可用于干燥,收集Cl2,并吸收多余的Cl2 |
| D.装置④配制一定物质的量浓度的溶液时转移液体 |
下列叙述正确的是
| A.一定温度、压强下,气体体积由其分子的大小决定 |
| B.一定温度、压强下,气体体积由其物质的量的多少决定 |
| C.气体摩尔体积是指1mol任何气体所占的体积为22.4L |
| D.不同的气体,若体积不等,则它们所含的分子数一定不等 |