下列氧化还原反应的离子方程式中正确的是……( )
| A.Cl2+6OH-=Cl-+ClO3-+3H2O | B.2Cl2+6OH-=3Cl-+ClO3-+3H2O |
| C.3Cl2+6OH-=5Cl-+ClO3-+3H2O | D.4Cl2+6OH-=7Cl-+ClO3-+3H2O |
在KClO3+6HCl==3Cl2↑+ KCl+3H2O中,有30 mole-转移,生成的氯气在标准状况下的体积为()
| A.22.4L | B.336.0L | C.403.2L | D.672.0L |
硫酸铵在强热条件下分解,生成氨、二氧化硫、氮气和水。反应中生成的氧化产物和还原产物的物质的量之比是()
| A.1:3 | B.2:3 | C.1:1 | D.4:3 |
今有0.1mol/L Na2SO4溶液300mL,0.1mol/L MgSO4溶液200mL和0.1mol/L Al2(SO4)3溶液100mL,这三种溶液中硫酸根离子浓度之比是()
A 1:1:1 B 3:2:1 C 3:2:3 D 1:1:3
设阿伏加德罗常数的值为NA,标准状况下某种O2和N2的混合气体mg含有b个分子,则ng该混合气体在相同状况下所占的体积应是()
A.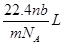 B.
B.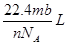 C
C 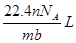 D.
D.
下面关于Na2CO3和NaHCO3性质的叙述,正确的是
| A.受热时NaHCO3比Na2CO3稳定 |
| B.在水中NaHCO3比Na2CO3溶解性大 |
| C.质量相等的Na2CO3和NaHCO3分别与足量盐酸反应,NaHCO3放出的CO2比Na2CO3多 |
| D.物质的量相等的Na2CO3和NaHCO3分别与足量盐酸反应,放出CO2的物质的量之比为2:1 |