从硫元素的化合价上判断,下列物质中的硫元素不能表现氧化性的是( )
| A.Na2S | B.S | C.SO2 | D.H2SO4 |
硒被称为主宰生命的元素之一,人们开发了一种含有钙铁锌硒(Ca、Fe、Zn、Se)的保健品。下列说法正确的是
| A.四种元素均处于第4周期,且均是主族元素 |
| B.H2Se比H2O热稳定性好 |
| C.单质钙能将FeSO4溶液中铁置换出来 |
D.与保健品中苏氨酸互为同分异构体的硝酸酯(RONO2)有四种 |
下列有关说法正确的是
| A.SO2(g)+H2O(g)→H2SO3(l),该过程熵值增大 |
| B.SO2(g)→S(s)+O2(g)△H>0,△S<0该反应能自发进行 |
| C.SO2(g)+2H2S(g)=3S(s)+2H2O(l) ,常温常压下一定能自发进行 |
D.某温度下SO2(g)+1/2O2(g)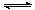 SO3(g),K1=20, SO3(g),K1=20, |
则相同温度下2SO3(g) 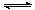 2SO2(g)+O2(g)的平衡常数为1/400
2SO2(g)+O2(g)的平衡常数为1/400
α-鸢尾酮香料的分子结构如右图,下列说法不正确的是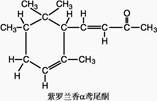
| A.α-鸢尾酮可与某种酚互为同分异构体 |
| B.1molα-鸢尾酮最多可与3molH2加成 |
| C.α-鸢尾酮能发生银镜反应 |
D.α-鸢尾酮经加氢→消去→加氢三步反应可转变为: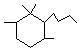 |
元素X的单质及X与Y形成的化合物能按如下图所示的关系发生转化。则X为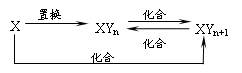
| A.当n=1时,X可能是C | B.当n=1时,X可能是N2 |
| C.当n=2时,X可能是S | D.当n=2时,X可能是Fe |
以下实验或操作不能达到目的的是
| A.用铜片(必要时可加热)鉴别浓硝酸、稀硝酸、浓硫酸和浓盐酸 |
| B.用品红溶液鉴别乙醛、苯、硝基苯 |
| C.用10mL量筒准确量取8.00mL1mol/L的KMnO4溶液 |
| D.用核磁共振氢谱图鉴别乙醇和甲醚 |